その理由は次のとおりです。
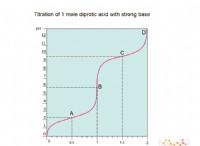
* pHスケール: pHスケールは、溶液の酸性度またはアルカリ度を測定します。 0から14の範囲で、
* 0-6: 酸性
* 7: 中性
* 8-14: ベーシック(アルカリ)
* ベースとpH: 塩基には水酸化物イオン(OH⁻)が含まれています。塩基が水に溶けると、これらの水酸化物イオンが放出されます。これらのイオンは、水中に存在する水素イオン(H⁺)と反応し、h⁺の濃度を減少させます。 pHはh⁺の濃度に反比例するため、H⁺の濃度が低いとpHが高いことを意味し、溶液がよりアルカリ性になります。
要約: 塩基は、水素イオン(H⁺)を中和する水酸化物イオン(OH⁻)を放出することにより、溶液のpHを増加させ、H⁺の濃度が低くなり、pHが高くなります。