その理由は次のとおりです。
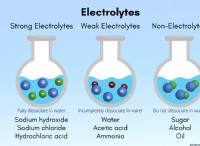
* 濃度: 濃度は、特定の量の溶媒または溶液に溶解する溶質の量を教えてくれます。濃度の一般的な単位には、モル濃度(リットルあたりのモル)、モル性(溶媒のキログラムあたりのモル)、および質量パーセント(溶液100グラムあたりの溶質のグラム)が含まれます。
* ボリューム: ボリュームだけで、ソリューションが占めるスペースの量を示しています。
水酸化ナトリウムのグラムを計算するには、以下を知る必要があります。
1。溶液の濃度: これは、モル濃度、モル性、または質量パーセントである可能性があります。
2。溶液の体積(m ml): この情報を提供しました。
例:
250 mLの体積を持つ水酸化ナトリウム(NAOH)の2 m(モル)溶液があるとしましょう。 Naohのグラムを計算する方法は次のとおりです。
1。モル濃度(m)=溶質のモル溶液 /溶液
2。 mlをリットルに変換: 250 ml =0.25リットル
3。 NaOHのモルを計算: (2モル/リットル) *(0.25リットル)=0.5モルnaOH
4。 naohのグラムを計算: (0.5モル) *(40 g/mole)=20グラムNaoh
したがって、20グラムのNaOHを250 mlの2 m NaOH溶液に溶解します。