これが故障です:
類似点:
* 溶解度: 同じ官能基を持つ化合物は、しばしば同様の溶解性パターンを示します。たとえば、アルカンよりもアルコールは水に溶けやすい傾向があります。
* 沸点: 同じ官能基を持つ化合物は、同様の分子量を持つアルカンと比較して、多くの場合、沸点が高いことがよくあります。これは、アルコール、ケトン、アルデヒドなどの官能基に存在するより強い分子間力によるものです。
違い:
* 分子量: 同じ官能基でさえ、異なる分子量の化合物は異なる沸点と融点を持ちます。一般に、より大きな分子は沸点と融点が高くなります。
* 分岐: 分子内での分岐は、分子間力の強度に影響を与え、沸点と融点に影響を与えます。枝分かれした分子が多く、沸点が低い傾向があります。
* 水素結合: 水素結合の存在と数は、沸点や溶解度などの物理的特性に大きく影響する可能性があります。たとえば、より多くのヒドロキシル基(OH)を持つアルコールは、より強力な水素結合を形成し、より高い沸点につながります。
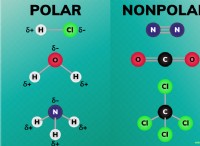
* 極性: 官能基や他の置換基の影響を受ける可能性のある分子の極性は、その溶解度と他の分子との相互作用に影響します。
例:
次のアルコールを検討してください。
* メタノール(CH3OH) :沸点が比較的低い小分子。
* エタノール(C2H5OH) :メタノールよりわずかに大きく、沸点がわずかに高い。
* 1-プロパノール(C3H7OH) :エタノールよりもさらに大きいため、沸点が高くなります。
3つはすべてアルコールであり、ヒドロキシル基(OH)により、特性の類似点を共有しています。しかし、それらの異なる分子量は、沸点に大きな違いをもたらします。
結論:
同じ官能基を持つ化合物はいくつかの類似点を共有していますが、その物理的特性は、分子量、分岐、極性などの他の要因にも影響されます。これらの要因は、機能グループ内の物理的特性の多様性に寄与します。