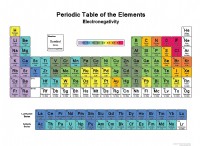
* イオン結合: イオン結合は、1つの原子(通常は金属)が電子を失い、正の帯電イオン(陽イオン)になると発生し、別の原子(通常は非金属)がそれらの電子を獲得して負に帯電したイオン(アニオン)になります。これらの反対に帯電したイオン間の強い静電引力は、イオン結合を形成します。
* 非金属特性: 非金属は電気陰性度が高いため、電子を引き付ける傾向があります。彼らは陽性イオンを形成するために電子を失うことを容易に喜んでいません。
* 共有結合: 2つの非金属が反応すると、電子を共有して共有結合を形成します。この共有は、イオン化合物ではなく分子を作成します。
例:
* ナトリウム(Na)および塩素(Cl): ナトリウムは金属であり、塩素は非金属です。それらは反応して、イオン化合物である塩化ナトリウム(NaCl)を形成します。
* 酸素(O)および水素(H): 酸素と水素はどちらも非金属です。それらは反応して、共有化合物である水(H2O)を形成します。
キーテイクアウト: イオン結合は、金属と非金属の間に形成されます。共有結合は、2つの非金属の間に形成されます。