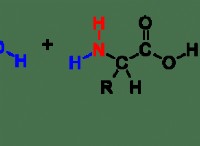
* 酢酸: ch3cooh。メチル基(CH3)は、電子誘発性であり、カルボキシル基(-COOH)に向かってわずかにプッシュ電子密度です。これにより、カルボキシル基の水素は酸性がわずかに少なくなります(H+として解離する可能性は低く)。
* ヨード酢酸: ICH2COOH。ヨウ素原子は非常に電気陰性であり、強力な電子吸引効果を持っています。カルボキシル基から電子密度を引き離し、カルボキシル基の水素をより酸性にします(H+として解離する可能性が高くなります)。
要約:
* 電子donatingグループ (メチルのように)減少 水素を離れる可能性が低くなることによる酸性度。
* 電子吸引グループ (ヨウ素のように)増加 水素を離れる可能性が高くなることによる酸性度。
これが、ヨード酢酸がより強い酸である理由です 酢酸より。