dative共有結合の特性:
座標結合とも呼ばれるデイティブ共有結合は、共有ペアの両方の電子が1つの原子によって寄付される特別なタイプの共有結合です。主要なプロパティの内訳は次のとおりです。
1。電子ペアの寄付:
* 1つの原子(ドナー)は、共有ペアに両方の電子を提供します。
*他の原子(アクセプター)は、寄付されたペアを収容するために空の軌道を提供します。
2。形成:
*多くの場合、ルイス酸(電子受容体)とルイスベース(電子ドナー)の間で発生します。
*ドナー原子には通常、孤立した電子のペアがあり、アクセプター原子には空いている軌道があります。
3。表現:
*ドナー原子からアクセプター原子を指す矢印で表されます。
*矢印は電子流の方向を表します。
4。強度:
*典型的な共有結合と強度が類似しています。
*強度は、参加している原子とその電気陰性度に依存します。
5。例:
* アンモニウムイオン(NH4+): 窒素(ドナー)は、その唯一のペアをプロトン(アクセプター)に寄付します。
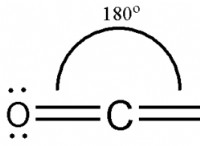
* 一酸化炭素(CO): 炭素(ドナー)は、酸素の空の軌道(アクセプター)に唯一のペアを寄付します。
* トリフルオリドボロン(BF3): フッ素(ドナー)は、ホウ素の空の軌道(アクセプター)に唯一のペアを寄付します。
6。通常の共有結合との区別:
*両方とも共有された電子ペアが含まれますが、dative共有結合では、1つの原子が両方の電子を提供します。
*通常の共有結合では、各原子は1つの電子を共有ペアに寄与します。
7。意味:
*安定した分子とイオンを作成できます。
*分子の形と反応性に影響を与える可能性があります。
8。化学の重要性:
*さまざまな化学反応やプロセスにおいて重要な役割を果たします。
*複合イオン、配位化合物、および多くの生物学的分子の形成に関与します。
全体的に、デイティブ共有結合は、化学結合の性質と分子とイオンの多様な構造と特性を理解する上で重要な概念です。