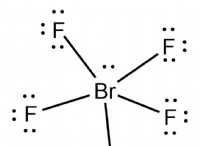
1。電子の共有:
*共有結合の決定的な特徴は、2つの原子間で電子を共有することです。
*この共有は、安定した電子構成を実現するために発生し、通常は貴族ガスの構成に似ています。
2。強い結合強度:
*共有結合は一般的に強力であり、壊れるのに大きなエネルギーが必要です。
*この強度は、共有電子と結合された原子の正に帯電した核との間の静電引力から生じます。
3。方向性:
*共有結合は方向性です。つまり、宇宙の特定の方向に発生します。
*この方向性は、結合に関与する電子軌道の形状の影響を受けます。
4。分子の形成:
*共有結合は、分子に原子をまとめる主要な力です。
*特定のプロパティを持つ離散的で識別可能なユニットを作成します。
5。結合タイプの汎用性:
*共有結合は、共有された電子ペアの数に応じて、単一、二重、トリプル結合を含むさまざまな形で存在できます。
*単一結合:1つの共有電子ペア。
*二重結合:電子の2つの共有ペア。
*トリプルボンド:電子の3つの共有ペア。
6。比較的低い融点と沸点(イオン化合物と比較):
*共有結合は強力ですが、分子間の力は比較的弱いです。これは、イオン化合物と比較して、共有化合物の融点と沸点が低くなります。
7。導電率が低い:
*共有化合物は、一般に、固体と液体の両方の電気の導体が貧弱です。これは、電子が共有結合内にしっかりと保持されており、自由に移動できるためです。
8。可変極性:
*共有結合は、極性または非極性のいずれかです。
*極性結合結合は、異なる電気陰性度の原子間で電子が不均等に共有され、部分的な正と負の電荷を生成するときに発生します。
*非極性共有結合は、電子が同様の電気陰性度を持つ原子間で等しく共有される場合に発生します。
9。有機化学にとって重要:
*共有結合は有機化学の基本であり、生物に見られるものを含む炭素ベースの分子の骨格を形成します。
10。多様なプロパティ:
*共有化合物は、原子の配置、結合の種類、および官能基の存在に影響される、広範囲の物理的および化学的特性を示します。
これらの特性は一般化であることに注意することが重要です。関係する特定の原子と分子構造に応じて、例外とバリエーションがあります。