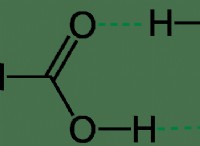
酸は、プロトン(H+)を別の物質(ベース)に寄付する物質です。
この定義が広く受け入れられている理由は次のとおりです。
* 普遍性: 水溶液や非水性環境のものを含む、広範囲の化学反応に適用されます。
* シンプルさ: 酸の挙動の重要な特徴、プロトンの寄付に焦点を当てています。
* 明確さ: 酸塩基反応を陽子の移動として理解するのに役立ちます。
酸の他の定義:
* arrhenius定義: 酸は、水に溶解すると水素イオン(H+)を生成する物質です。これは、水溶液にのみ適用されるため、より限られた定義です。
* ルイス定義: 酸は電子ペアアクセプターです。これは、必ずしも水素を含むものではない物質を含む、より一般的な定義です。
他の定義が存在しますが、Brønsted-Lowryの定義 最も一般的に使用されており、酸の挙動を理解するために最も包括的です。