* カチオン: これらは、原子が1つ以上の電子、通常は金属を失うと形成されます。例は次のとおりです。
*ナトリウム(Na+)
*カルシウム(Ca2+)
*アルミニウム(AL3+)
* アニオン: これらは、原子が1つ以上の電子、通常は非金属を獲得すると形成されます。例は次のとおりです。
*塩化物(CL-)
*酸化物(O2-)
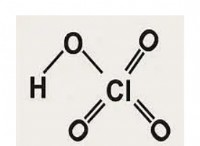
*硫酸塩(SO42-)
したがって、イオン化合物には一般的に含まれています。
* 金属 (陽イオンの形成)
* 非金属 (アニオンの形成)
重要な注意: 次のようないくつかの例外があります。
* 多原子イオン: これらは、正味電荷を持つ単一のユニットとして機能する原子のグループです。それらは陽イオンまたはアニオンのいずれかであり、多くの場合、金属と非金属の両方を含むことができます(例:アンモニウムイオンNH4+、炭酸イオンCO32-)
* 遷移金属: これらは、異なる電荷で複数の陽イオンを形成することができます(たとえば、鉄はFe2+またはFe3+を形成できます)。
全体として、イオン化合物の基本的な成分は、電子(陽イオン)を失う金属と電子(アニオン)を獲得する非金属です。これらの反対に帯電したイオンは互いに引き付けられ、イオン結合が生じます。