1。 溶質と溶媒の性質:
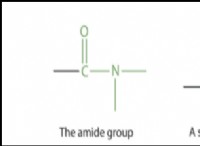
* "like like dislols like": 極性溶質は極性溶媒に溶解し、非極性溶質は非極性溶媒に溶解します。
* 例: 砂糖(極)は水(極)によく溶解しますが、油(非極性)には溶けません。
* 例: オイル(非極性)はガソリン(非極性)によく溶解しますが、水(極)には溶解しません。
* 分子間力: 溶質分子と溶媒分子の間の分子間力が強いほど、溶解度が高くなります。
* 例: NaClのようなイオン化合物は強いイオン結合を持っていますが、水分子がイオンとの強い双極子イオン相互作用を形成できるため、水によく溶解します。
2。温度:
* 固体と液体: 一般に、温度が上昇すると溶解度が増加します。より多くの熱エネルギーは、溶質分子間の結合を破壊し、溶媒と相互作用する可能性が高くなります。
* ガス: 温度が上昇すると溶解度が低下します。 ガス分子は、より多くの運動エネルギーを持っているときに溶解する可能性が低くなります。
3。圧力:
* ガス: 溶解度は、圧力の増加とともに増加します。 より高い圧力により、より多くのガス分子が溶液になります。
4。粒子サイズ:
*より小さな粒子は、表面積と体積比が高いため、大きな粒子よりも速く溶解します。これにより、溶媒との接触が増えます。
5。攪拌または動揺:
*新鮮な溶媒分子を溶質と接触させることにより、攪拌または攪拌により溶解が高速化されます。
溶解度の測定:
* 溶解度は通常、特定の温度で溶媒100グラムあたりの溶質グラムで表されます。
追加ポイント:
* 飽和: 溶液が特定の温度で最大量の溶質を保持すると、飽和と言われます。
* 過飽和: 特定の条件下では、溶液は通常の溶解度制限よりも溶質を保持できます。これはメタスト可能な状態であり、簡単に破壊することができます。
要約すると、物質の溶解の容易さは、その化学的性質、溶媒の種類、温度、圧力、粒子サイズ、および攪拌に依存します。