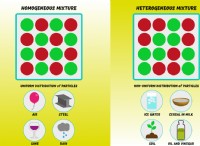
中和反応の例
中和反応には、酸と塩基の間の反応が含まれ、塩と水が形成されます。ここにいくつかの例があります:
1。強酸と強いベース:
* 塩酸(HCl) +水酸化ナトリウム(NAOH)→塩化ナトリウム(NaCl) +水(H2O)
*これは、強酸(HCl)が強力なベース(NAOH)と反応して中性塩(NaCl)と水を形成する古典的な例です。
2。弱酸と強いベース:
* 酢酸(CH3COOH) +水酸化ナトリウム(NAOH)→酢酸ナトリウム(CH3COONA) +水(H2O)
*ここでは、弱酸(酢酸)が強い塩基(NaOH)と反応して、塩(酢酸ナトリウム)と水を生成します。
3。強酸と弱い塩基:
* 塩酸(HCl) +アンモニア(NH3)→塩化アンモニウム(NH4Cl)
*この例では、強酸(HCl)が弱い塩基(アンモニア)と反応して、塩(塩化アンモニウム)と水を形成します。
4。弱酸と弱い塩基:
* 酢酸(CH3COOH) +アンモニア(NH3)→酢酸アンモニウム(CH3COONH4)
*この反応には、弱酸(酢酸)と弱い塩基(アンモニア)が含まれ、塩(酢酸アンモニウム)と水を形成します。
5。炭酸塩との反応:
* 塩酸(HCl) +炭酸カルシウム(CACO3)→塩化カルシウム(CACL2) +二酸化炭素(CO2) +水(H2O)
*炭酸塩は酸と反応して二酸化炭素、塩、水を生成します。
6。重炭酸塩との反応:
* 塩酸(HCl) +重炭酸ナトリウム(NAHCO3)→塩化ナトリウム(NaCl) +二酸化炭素(CO2) +水(H2O)
*重炭酸塩も酸と反応して二酸化炭素、塩、水を生成します。
7。生物学的例:
* 制酸剤による胃酸の中和: 炭酸カルシウム(CACO3)のような制酸剤は、胃酸(HCl)と反応してそれを中和し、胸焼けを緩和します。
* 体内のバッファシステム: 血液には、酸と塩基を中和するバッファシステムが含まれており、安定したpHを維持します。
これらは、中和反応のほんの一例です。それらは、日常生活から生物学的プロセスまで、さまざまな文脈で頻繁に発生します。