電気陰性度の基本:
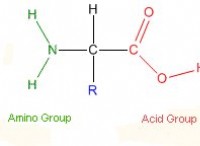
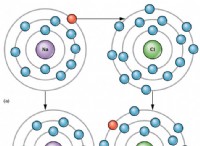
* 定義: 電気陰性度は、化学結合内で電子を引き付ける原子の能力です。
* 定期的な傾向: ピリオド(左から右)に移動し、周期表のグループを上に移動すると、電気陰性度が増加します。
水の分子構造:
* 構成: 水(H₂O)は、2つの水素原子と1つの酸素原子でできています。
* 曲がった形: 分子の形状は曲がっており、酸素原子は中心にあり、水素原子は約104.5度の角度を形成します。
水中の電気陰性度:
* 酸素のプル: 酸素は水素よりも有意に電気陰性です。これは、酸素がO-H結合の共有電子をより強く引っ張っていることを意味します。
* 不均一な共有: 電子は酸素原子の近くでより多くの時間を費やし、わずかに負電荷(Δ-)を与え、水素原子にわずかに正電荷(Δ+)を残します。
* 双極性自然: この不均一な電荷分布は、水分子内に永久双極子モーメントを作成します。
結果の極性:
* アトラクション: ある水分子の正の端は、別の水分子の負の端に引き付けられます。
* 水素結合: この魅力は水素結合と呼ばれ、その高い沸点、表面張力、多くの物質を溶解する能力など、水のユニークな特性の多くを担当しています。
要約: 酸素原子のより高い電気陰性度がO-H結合の共有電子をそれに近づけ、酸素に部分的な負電荷と水素原子の部分的な正電荷を引き出すため、水は極性分子です。この不均一な電荷分布は、永続的な双極子モーメントを作成し、水を極分子にします。