安定した分子の重要な特性を次に示します。
* 強い債券: 安定した分子には、原子間に強い結合があります。つまり、それらを破るにはかなりの量のエネルギーが必要です。
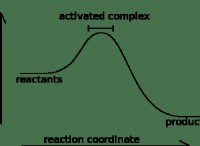
* 低エネルギー状態: それらは、構成要素の原子と比較して低エネルギー状態を持っています。つまり、より安定しており、反応を起こす可能性が低くなります。
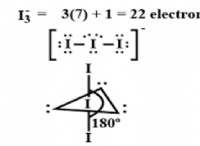
* 好ましい電子構成: 安定した分子の電子は、原子が8つの原子価電子を持つまで電子を獲得、失い、または共有する傾向があると述べるオクテットのルールを満たす方法で配置されます。
* バランス料金: 分子内の電荷は均等に分布しており、中性またはわずかに偏光状態を作成します。
安定した分子の例:
* 水(h₂o): 強い共有結合とバランスの取れた電荷分布を備えた非常に安定した分子。
* 二酸化炭素(CO₂): その強い二重結合と低エネルギー状態により、別の非常に安定した分子。
* 窒素ガス(n₂): 窒素原子の間に強い三重結合を持つ非常に安定した分子。
安定性に影響する要因:
* 結合強度: 強い結合は安定性の向上につながります。
* 電子構成: 満たされた外側の電子シェル(オクテットルール)は、安定性に寄与します。
* 極性: 非極性分子は一般に極性分子よりも安定しています。
* 温度: より高い温度は分子を不安定にすることができます。
* 触媒の存在: 触媒は、分解速度を加速できます。
安定性は相対概念であることに注意することが重要です 。 安定性の絶対スケールはありません。一部の分子は、特定の条件下で他の分子よりも単純に安定しています。