その理由は次のとおりです。
* 酸化状態 すべての結合が100%イオンである場合、原子が持つ仮想電荷を表します。
* 孤独 他の原子に結合されていません。考慮すべき結合がないため、酸化状態は0です。
* ガス中の原子 多くの場合、単一の原子または珪藻類分子(酸素ガス、O₂など)として見られます。 これらの場合、原子は電子を等しく共有しているため、正味電荷がなく、酸化状態は0です。
例:
* ヘリウム(彼) :単一の原子として見つかった貴重なガス。酸化状態=0。
* 窒素(n₂) :二原子分子。各窒素原子の酸化状態=0。
* 酸素(o₂) :二原子分子。各酸素原子の酸化状態=0。
例外:
ガス中のほとんどの孤立元素と原子の酸化状態は0ですが、いくつかの例外があります。これらは通常、次のような異常な状況で見られます。
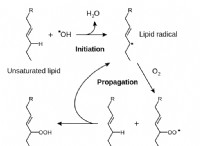
* 反応性ラジカル :これらは、不対の電子を持つ原子または分子であり、それらを非常に反応性にすることができます。それらの酸化状態は0ではない場合があります。
* 特定の化合物のガス :唯一の要素または原子がより大きな化合物の一部である場合、その酸化状態は、その化合物内で形成される結合によって決定されます。
他に質問がある場合はお知らせください!