極粒子:
* 充電の不均一な分布: 分子の一方の端はわずかに正電荷(Δ+)を持ち、もう一方の端にはわずかに負の電荷(Δ-)があります。これは、分子内の原子間の電気陰性度の違いが原因で発生します。 電気陰性度とは、原子がそれ自体に電子を引き付ける傾向です。
* 双極子モーメント: 極性分子には永久的な双極子モーメントがあり、これは正電荷と負の電荷の分離の尺度です。
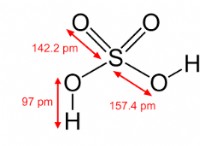
* 例: 水(h₂o)。酸素は水素よりも電気陰性であるため、共有電子をより強く引き付け、酸素原子に部分的な負電荷と水素原子の部分的な正電荷を生成します。
非極性粒子:
* 電荷の均一な分布: 電子は、分子の原子間で均等に共有されます。これは、原子が同様の電気陰性度を持っているときに起こります。
* 双極子モーメントなし: 非極性分子には永久的な双極子モーメントはありません。
* 例: メタン(ch₄)。炭素と水素は同様の電気陰性度を持っているため、電子は均等に共有され、バランスの取れた電荷分布が生じます。
重要な違い:
|機能|極粒子|非極性粒子|
| --- | --- | --- |
|充電分布|不均一| |
|双極子モーメント|存在|不在|
|電気陰性度の差|高|低|
|相互作用|強い分子間力(水素結合、双極子型双極子相互作用)|弱い分子間の力(ロンドン分散力)|
|溶解度|一般に、極性溶媒(水)に溶けます|一般に、非極性溶媒(油など)に溶けます|
ここに簡単なアナロジーがあります: 不平等な強さの2つのチームの間の綱引きを想像してください。より強いチームは、ロープをさらに彼らの側に向けて引っ張り、ロープの不均一な分布をもたらします。これは極性分子に似ており、電気陰性の原子が電子をそれ自体に近づけ、不均一な電荷分布を作成する極性分子に似ています。
非極性分子では、等しい強度の2つのチームがロープを引っ張るようなものであり、その結果、ロープが均等に分布します。 これは、原子が同様の電気陰性度を持ち、電子の均等な分布につながる非極性分子に似ています。