* 陽子: 原子核に位置する正に帯電した粒子。
* 中性子: 中立帯電した粒子も核に位置しています。
* 電子: 電子シェルと呼ばれる雲のような領域で核を周回する負に帯電した粒子。
これがそれぞれの内訳です:
陽子:
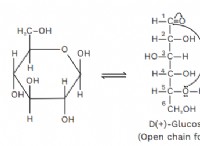
*要素を決定する:原子の核内の陽子の数は、それがどの要素であるかを定義します。たとえば、すべての炭素原子には6つのプロトンがあります。
*核に位置する:中性子とともに、陽子は原子の密な、正に帯電した中心を形成します。
*電子に等しい:中性原子では、プロトンの数は電子の数に等しくなります。
中性子:
*電荷なし:中性子には電荷がありません。
*核に位置する:それらは原子コアの陽子と一緒に住んでいます。
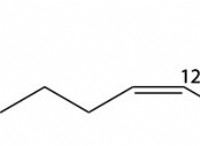
*影響同位体:プロトンの数は元素を定義しますが、中性子の数はその要素の同位体を決定します。たとえば、炭素12と炭素-14は炭素の同位体であり、中性子の数のみが異なります。
電子:
*負に帯電した:電子は負電荷を運びます。
*核を周回する:それらは、特定のエネルギーレベルで、電子シェルと呼ばれる核の周りの雲のような領域に存在します。
*結合に関与する:原子電子と呼ばれる最も外側のシェルの電子は、原子間の化学結合の原因です。
要約:
原子は、負に帯電した電子の雲に囲まれた陽子と中性子を含む核で構成されています。これらの粒子の配置と相互作用は、各要素の固有の特性と物質の複雑さを生じさせます。