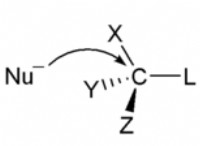
その理由は次のとおりです。
* 同じ数の陽子と電子: 塩素-35と塩素-37の両方に、17個のプロトンと17個の電子があります。 This means they have the same electronic configuration and identical reactivity.
* 中性子は化学結合に関与していません: 2つの同位体の違いは、中性子の数にあります(塩素-35で18、塩素-37で20)。中性子は核内に位置し、電子間で発生する化学結合に関与しません。
ただし、質量の違いによる反応には微妙な違いがあります:
* 速度論的同位体効果: 質量のわずかな違いにより、塩素-35と塩素-37は、特定の反応でわずかに異なる反応速度を持つ可能性があります。これらの違いは通常小さく、特定の状況でのみ顕著です。
* 分光違い: 同位体は、分子の振動周波数など、わずかに異なる分光特性を示すこともできます。
要約: 塩素同位体の挙動には微妙な違いがありますが、その化学反応性は、陽子と電子の同一数のために本質的に同じです。中性子の数の違いは、化学的結合と挙動に無視できる影響を及ぼします。