化学組成の変化:
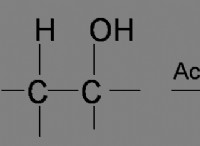
* 新しい物質の形成: 反応物(出発材料)は、異なる化学的特性を持つまったく異なる製品に変換されます。これには、化学結合の破壊と形成が含まれます。
* 原子の再配置: 反応物内の原子は再配置され、新しい分子を形成します。
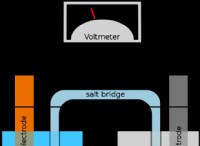
* 酸化状態の変化: 原子は電子を獲得または失い、酸化状態を変更する場合があります。
エネルギーの変化:
* エネルギーの放出(発熱反応): 反応は周囲に熱を放出し、しばしば温度を上昇させます。
* エネルギーの吸収(吸熱反応): 反応は周囲から熱を取り、しばしば温度を下げます。
物理的な変化:
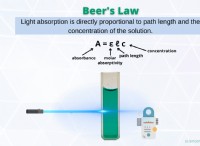
* 色の変化: 物質の外観は劇的に変化する可能性があり、新しい化合物が形成されたことを示しています。
* 沈殿物の形成: ソリューションから固体製品が形成されます。
* ガスの進化: ガスバブルは環境に放出されます。
* 臭いや味の変化: 製品は、反応物と比較して明確な臭いや味を持っている可能性があります。
その他の現象:
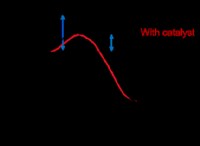
* 触媒の関与: 触媒は、プロセスで消費されることなく反応速度を高速化します。
* 平衡: 順方向反応と逆反応の速度が等しい状態であり、その結果、反応物と生成物が一定の濃度が生じます。
* 副反応: 不要な反応は、主な反応とともに発生する可能性があり、望ましくない製品を生成します。
重要なメモ:
* 化学反応は、質量の保全法則によって支配されています: 反応物の総質量は、製品の総質量に等しくなければなりません。
* 化学式は変化を表します: それらは、反応物と生成物の化学式、およびそれぞれの化学量論(相対量)を示しています。
これらの側面を理解することは、薬、産業、日常生活など、多くの分野で不可欠な化学反応の結果を予測および制御するのに役立ちます。