1。安定性:
* 電気陰性度: 原子は、より安定した電子構成を実現するために再配置する傾向があります。これには、一般的に最も安定した状態と見なされる電子の完全な外殻を達成することがよくあります。
* オクテットルール: 原子は、電子を獲得、失い、または共有する傾向があり、最も外側のシェル内の8つの電子の安定した構成に到達する傾向があります。 このルールは、最初の3つの期間内の要素で特に顕著です。
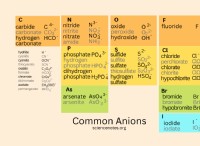
* イオン結合: 原子の電気陰性度に大きな違いがある場合、ある原子は電子を別の原子に伝達し、互いに引き付ける反対の電荷を持つイオンを作成できます。これはイオン化合物を形成します。
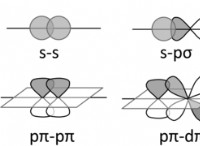
* 共有結合: 原子が同様の電気陰性度を持っている場合、安定性を達成するために電子を共有できます。これは共有結合を形成し、分子の形成につながります。
2。エネルギー最小化:
* 化学反応: 原子は再配置して、エネルギー状態が低い新しい物質を形成します。エネルギーのこの放出は、化学反応を促進し、多くの化学現象の基礎となります。
* 結合エネルギー: さまざまな結合には強みが異なり、反応はより強力な結合の形成を支持する傾向があります。これはエネルギー状態が低いためです。
3。環境要因:
* 温度: 熱は、反応が発生するのに必要な活性化エネルギーを克服できるエネルギーを提供します。 より高い温度は、より迅速な再配列につながる可能性があります。
* 圧力: 圧力の変化は、化学反応の速度と方向に影響を与え、原子の再配置に影響を与えます。
* 触媒: 触媒は、消費されることなく化学反応を高速化する物質です。それらは、原子再配置のための代替経路を提供し、より速く、より効率的な反応につながることができます。
4。ランダム性と確率:
* 衝突理論: 化学反応は、反応物分子が十分なエネルギーと適切な方向と衝突すると発生します。このランダム性は、さまざまな再配置の可能性につながる可能性があります。
要約すると、原子は、安定性、エネルギーの最小化、環境要因の影響によって駆動される要因の組み合わせのために、新しい物質を形成するために再配置して新しい物質を形成します。