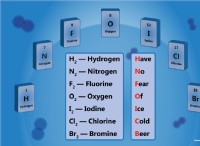
* 酸素(O) 外側のシェルに6つの電子があり、安定した構成を実現するにはさらに2つが必要です。
* 水素(H) 外側のシェルに1つの電子があり、もう1つが安定する必要があります。
酸素は2つの外部電子を2つの水素原子と共有し、 2つの共有結合を形成します 。各水素原子は、その単一電子を酸素原子と共有しています。
この電子の共有は、強い結合を作成します 水素と酸素原子の間で、水分子を形成します。
重要な注意: 共有は等しくありません。酸素はより電気陰性であるため、電子をより強く引き付けることを意味します。これにより、水分子の酸素側がわずかに陰性(Δ-)になり、水素側がわずかに正(Δ+)になります。この不均一な電荷分布は、水をその極性の性質に与え、水素結合のような他の重要な特性につながります。