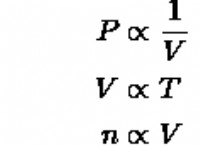これは化学の基本的な関係であり、水のイオン産物(KW)に由来します。
* kw =[h+] [oh-] =1.0 x 10^-14 25°Cで
どこ:
* [H+]は水素イオン濃度です
* [OH-]は水酸化物イオン濃度です
方程式の両側の負の対数を使用すると、次のことが得られます。
* -log(kw)=-log([h+] [oh-])
* -log(kw)=-log [h+] - log [oh-]
* pkw =ph + poh
pkwは-log(1.0 x 10^-14)=14であるため、次のようになります。
ph + poh =14
この方程式は、25°Cのすべての水溶液に当てはまります。