同位体
* 定義: 同じ数の陽子(原子数)があるが、異なる数の中性子を持つ同じ元素の原子。
* キー機能: 彼らは同じ化学的挙動を持っていますが、異なる原子質量を持っています。
* 例: 炭素-12(6陽子、6個の中性子)および炭素-14(6陽子、8個の中性子)は炭素の同位体です。
イオン
* 定義: 電子を獲得または失った原子または分子により、正味の電荷が生じます。
* キー機能: それらは、陽子と電子の数の不均衡のために、正の(陽イオン)または陰性(陰イオン)電荷を持っています。
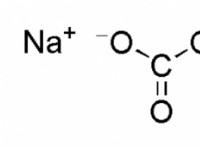
* 例: ナトリウムイオン(Na+)は1つの電子を失い、塩化物イオン(Cl-)は1つの電子を獲得しました。
分子
* 定義: 化学結合によって結合された2つ以上の原子。
* キー機能: それらは、同じ要素(酸素ガス、O2など)または異なる要素(水、H2Oなど)で構成できます。
* 例: 水(H2O)は、2つの水素原子と1つの酸素原子によって形成される分子です。
テーブルの重要な違い:
|機能|同位体|イオン|分子|
| ---------------- | ------------- | ------------- | ------------------- |
| 定義 |同じ要素、異なる中性子|帯電した原子/分子|結合した2つ以上の原子|
| 変更 |中性子の数|電子の数|原子の数|
| 電荷 |ニュートラル|正または負|ニュートラル|
| 化学的挙動 |同様の|異なる|異なる|
要約:
* 同位体 中性子数が異なり、質量に影響します。
* イオン 電子数が異なり、電荷につながります。
* 分子 原子の結合によって形成されます。
これらの概念のいずれかについてもっと詳細をご希望の場合はお知らせください!