その理由は次のとおりです。
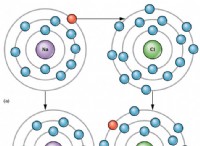
* 低イオン化エネルギー: これらの金属はイオン化エネルギーが低いため、外側のシェルから電子を除去するには比較的少ないエネルギーが必要です。これにより、彼らは電子を失い、正のイオンを形成したいと考えています。
* 大きな原子半径: これらのグループの原子には大きな原子半径があります。これは、外側の電子が核から遠く、硬く保持されていないため、除去が容易になることを意味します。
反応金属の例:
* グループ1(アルカリ金属): リチウム(Li)、ナトリウム(NA)、カリウム(K)、ルビジウム(RB)、セシウム(CS)、フランシウム(FR)
* グループ2(アルカリアース金属): ベリリウム(BE)、マグネシウム(MG)、カルシウム(CA)、ストロンチウム(SR)、バリウム(BA)、ラジウム(RA)
重要な注意: グループを下に移動すると、反応性が増加します。 たとえば、フランシウムは最も反応性の高い金属です。