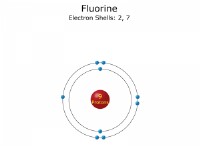
これがBohrモデルの内訳です:
重要な機能:
* 核: 陽子と中性子を含む原子の核は、密集した積極的に帯電したコアと見なされます。
* 電子軌道: 電子は、星を周回する惑星のように、特定の円形軌道で核の周りを回転します。これらの軌道は量子化されています。つまり、電子は特定のエネルギーレベルでのみ存在できます。
* 量子化されたエネルギーレベル: BOHRモデルは、電子は整数(n =1、2、3など)で示される特定のエネルギーレベルでのみ存在できると述べています。 最も低いエネルギーレベル(n =1)は基底状態であり、より高いレベルは励起状態を表します。
* 電子遷移: 電子は、光の光子を吸収または放出することにより、エネルギーレベルの間をジャンプできます。電子が光子を吸収すると、エネルギーを獲得し、より高いエネルギーレベルに移動します。電子が光子を放出すると、エネルギーを失い、低いエネルギーレベルに低下します。放出された光子のエネルギーは、2つのレベル間のエネルギーの違いに対応します。
bohrモデルの強度:
* 原子の線スペクトルについて説明します: BOHRモデルは、エネルギーレベル間の電子が遷移するときに放出される水素原子の観測されたラインスペクトルを正常に説明しました。
* 原子構造の基本的な理解を提供します: それは、原子の挙動を理解するための基本的な量子化されたエネルギーレベルと電子軌道の概念を導入します。
bohrモデルの制限:
* 水素様原子にのみ適用されます: BOHRモデルは、水素のスペクトル線を正確に予測しますが、複数の電子を持つ原子のスペクトルを予測できません。
* 電子スピン:は説明していません このモデルは、電子の固有の角運動量(スピン)を考慮していません。これは、その行動を理解するために重要です。
* 古典的なメカニックモデル: このモデルは、原子の量子性と根本的に互換性がない古典的なメカニズムに基づいています。電子は、惑星のような明確に定義された軌道で動きません。
概要:
BOHRモデルは、原子構造の基本的な理解を提供する単純化されたが歴史的に重要なモデルです。制限がありますが、現代の原子理論の基礎を形成する量子化エネルギーレベルや電子遷移などの重要な概念を導入しました。
BOHRモデルは、原子の完全または正確な描写ではないことを覚えておくことが重要です。原子内の電子の複雑な挙動を記述するには、量子機械モデルのようなより洗練されたモデルが必要です。