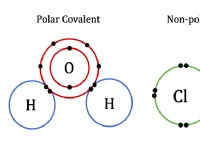
溶解度に影響する要因:
* 極性: 水は非常に極性分子です。正の端(水素)と負の端(酸素)があります。 同様の極性の物質は、水に溶ける傾向があります。
* 極地 (砂糖、塩、アルコールなど)分子が水分子と水素結合を形成できるため、水によく溶解します。
* 非極性化合物 (オイル、脂肪、ワックスなど)これらの結合を形成する能力がないため、水に溶けません。
* 分子間力: 化合物内のより強力な分子間力は、水分子が化合物の構造を分解することを難しくすることができます。
不溶性化合物の例:
* ほとんどの炭化水素: これらは、炭素と水素のみで構成される化合物であり、一般に非極性です。例は次のとおりです。
*オイル
*脂肪
*ワックス
*ガソリン
* 多くの塩: 一部の塩は可溶性(テーブル塩のような)が、他の塩は不溶です。
*炭酸カルシウム(チョーク)
*塩化銀
* いくつかの金属: ほとんどの金属は水に不溶です。
重要な注意: 「可溶性」と「不溶性」という用語は相対的です。 技術的には、完全に不溶性の物質のようなものはありません。最も不溶性化合物でさえ、水に少し溶けます。