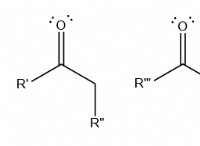
原子とその外側のエネルギーレベル(価数シェル)
* 原子 物質の基本的な構成要素です。それらは、特定のエネルギーレベルの電子に囲まれた陽子と中性子を含む中央の核を持っています。
* 最も外側のエネルギーレベル(価数シェル): これは、電子が化学反応に関与する可能性が最も高いエネルギーレベルです。 このシェルの電子の数は、原子の反応性を決定します。
外側のエネルギーレベルでの原子の共有:共有結合
* 共有結合 原子が原子価殻内の電子を共有する化学結合の一種です。この共有により、各原子は、Nobleガスのようなより安定した電子構成を実現できます。
* 例:水分子(H₂O)
*酸素(O)には、その原子価シェルに6つの電子があり、安定するためにさらに2つの電子が必要です。
*水素(H)には、価数シェルに1つの電子があり、安定するためにさらに1つの電子が必要です。
*水中では、各水素原子はその1つの電子を酸素原子と共有し、酸素原子は各水素原子とその電子の1つを共有します。これにより、各水素と酸素原子の間に共有電子ペアを持つ安定した分子が生成されます。
共有が重要な理由:
* 安定性: 電子を共有することにより、原子はより安定した電子の構成を実現でき、多くの場合、貴族の構成に似ています。これは、化学結合の基本的な原動力です。
* 分子の形成: 共有結合は、水、二酸化炭素、無数の有機分子を含む多くの分子の形成の基礎です。
* 多様なプロパティ: 共有結合の種類と配置は、分子に独自の特性を与えます。
キーポイント:
*共有結合中の電子の共有は、原子がどのように相互作用して新しい物質を形成するかの重要な側面です。
*この共有は、関与する原子の安定性の向上につながります。
*共有結合は、多様な特性を持つ分子の膨大な配列の形成を担当します。
さまざまな種類の化学結合や、電子を共有することによって形成された分子の例についてもっと探求したい場合はお知らせください!