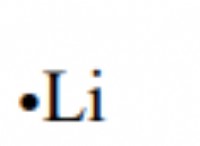原子価電子と貴族:緊密な関係
価電子 原子の最も外側のエネルギーレベルの電子です。それらは、他の原子と最も簡単に獲得、紛失、または共有されるため、化学的結合に関与するものです。
nobleガス 、不活性ガスとしても知られているのは、周期表の要素のグループであり、非常に反応しません。これは、彼らが電子の完全な外側の殻を持っているためです。つまり、 8価電子 (2つのヘリウムを除く)。
これらがどのように関連するかは次のとおりです。
* 安定性: ノーブルガスは、外側の殻がいっぱいであるため、非常に安定しており、この安定した状態を達成するために電子を獲得または失う必要はありません。
* 反応性: 他の要素は、貴族と同様の安定した電子構成を実現できるように反応する傾向があります。これは、オクテットルールの基礎です 、原子は、8電子の完全な外殻を達成するために電子を獲得、失い、または共有する傾向があると述べています。
* 結合: 原子の原子価の数は、それが他の原子とどのように結合するかを決定します。たとえば、1〜3個の原子価電子を持つ元素は、それらを失い、陽性イオンを形成する傾向がありますが、5〜7個の原子価電子を持つ元素は、陰イオンを形成するために電子を獲得する傾向があります。
これが簡単な類推です:ビー玉の完全な瓶を想像してください。それは安定しており、これ以上の大理石は必要ありません。 今、いくつかの不足している瓶を想像してみてください。これらの瓶は安定性が低く、より多くのビー玉を手に入れたり、瓶のようになったりしなければならないものをあげようとします。
それが高貴なガスと価電子の働きです!それらは、化学的結合と元素の反応性を理解するための鍵です。