1。価電子:
* 炭素: 4つの価電子があります。つまり、安定したオクテット構成を実現するために4つの結合を形成できます。これにより、非常に用途が広く、さまざまな要素と結合できます。
* 水素: 1つの価電子があり、安定したデュエット構成を実現するために1つの結合を形成します。
* 酸素: 6つの価電子があり、安定したオクテット構成を実現するために2つの結合を形成します。
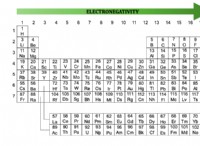
2。電気陰性度:
* 炭素: 中程度の電気陰性度があり、それ自体を含む広範囲の要素と共有結合を形成することができます。
* 水素: 電気陰性度が低いため、酸素のようなより多くの電気性要素と共有結合を形成する可能性が高くなります。
* 酸素: 電気陰性度が高いため、炭素や水素などの電気陰性要素が少ない共有結合を形成する可能性が高くなります。
3。化学結合:
* 共有結合: これらの3つの要素は主に共有結合を形成し、そこでは電子が原子間で共有され、安定した構成を実現します。
* イオン結合: あまり一般的ではありませんが、酸素は、ナトリウム(NA)のような高度な電気依存症の元素とイオン結合を形成することがあります。
4。自然の豊かさ:
* 炭素、水素、酸素 宇宙と地球上で最も豊富な要素の1つです。この豊富さにより、他の要素に遭遇して化合物を形成する可能性が統計的に可能になります。
化合物の例:
* 水(H2O): 水素と酸素は強い共有結合を形成します。
* 二酸化炭素(CO2): 炭素は、2つの酸素原子と二重結合を形成します。
* 砂糖(C6H12O6): 炭素、水素、酸素はさまざまな比率で結合し、複雑な炭水化物を形成します。
要約: それらの原子価電子、電気陰性度、および共有結合を形成する傾向の組み合わせにより、炭素、水素、酸素が非常に反応し、他の要素と結合する可能性が高くなり、生命と自然界に不可欠な多様な化合物を形成します。