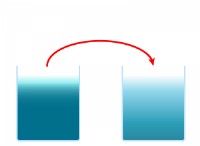
p₁v₁=p₂v₂
どこ:
* p₁ 初期圧力です
* v₁ 初期ボリュームです
* p₂ 最終的な圧力です
* v₂ 最終ボリュームです
これが起こる理由は次のとおりです。
* ガス分子は一定の動きです: 彼らは互いに衝突し、容器の壁に衝突します。
* 圧力は、これらの衝突によって引き起こされます: より頻繁な衝突は、より高い圧力を意味します。
* ボリュームの減少により衝突が増加します: ガスをより小さなスペースに絞ると、分子は動き回る余地が少なくなり、容器の壁とより頻繁に衝突します。これにより、圧力が増加します。
* ボリュームの増加により衝突が減少します: 逆に、ガスの体積を拡大すると、分子の空間が増え、衝突の頻度が減少し、圧力が低下します。
例:
* タイヤの膨張: 空気をタイヤに送り込むと、より多くの空気分子を同じ量に強制するため、圧力が増加します。
* 注射器を押し下げる: シリンジのプランジャーを押すと、内部の空気の体積が減少し、圧力が増加します。
重要な注意: この関係は、温度とガスの量が一定のままである場合にのみ当てはまります。これらの要因のいずれかが変化すると、体積と圧力の関係が影響を受けます。