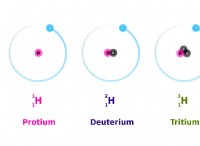
1。水の極性:
*水分子は非常に極性です。つまり、正の末端(水素原子)と負の末端(酸素原子)があります。
*この極性により、水分子は互いに強い水素結合を形成することができます。
2。極性への非極性ガスの無関心:
*窒素(N2)、酸素(O2)、メタン(CH4)などの非極性ガスは、有意な電荷分離を欠いています。
*それらは水素結合を形成せず、分子間力(van der waals力)が弱い。
衝突:
*非極性ガス分子が水に溶解しようとすると、水分子を一緒に保持している水素結合の複雑なネットワークが混乱します。
*非極性ガス分子に対応するには、水分子が強い水素結合を弱め、ガスとの弱い相互作用を形成する必要があります。
*これは、水素結合を破るにはエネルギーが必要なため、エネルギー的に好ましくありません。
結果:
*システムは、水中の非極性ガスの溶解度を制限することにより、破壊を最小限に抑えます。
*油と水を混ぜようとするようなものです。分子の相互作用が互換性がないため、2つの物質が容易に混ざりません。
このように考えてみてください: 手をしっかりと握っている人々のグループ(水分子)を想像してください。さて、まったく異なる関心のある人(非極性ガス)をグループに絞るようにしてください。彼らは同じ接続を共有していないので難しいです。