何が起こるか:
* 酸 水素イオン(H+)を溶液に放出します。
* ベース 水酸化物イオン(OH-)を溶液に放出します。
* 酸と塩基が混ざると、H+とOH-イオンが組み合わせて水を形成します(H2O):
H + + OH-→H2O
* 酸と塩基からの残りのイオンは塩を形成します:
たとえば、塩酸(HCl)が水酸化ナトリウム(NAOH)と反応する場合:
HCl + NaOH→H2O + NaCl(塩化ナトリウム、テーブル塩)
キーポイント:
* 中和により、pHが7(ニュートラル)に近い溶液が生じます。
* 形成された塩は、しばしば水に溶けます。
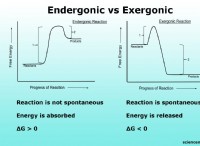
* 反応は熱を放出し、発熱反応にします。
例:
酢(酢酸)と重曹(重炭酸ナトリウム)と混合することを考えてください。 この反応は、二酸化炭素ガス(泡)、水、および酢酸ナトリウム(塩)を生成します。
特定の例を調べたい場合はお知らせください。