コア コンセプト
このチュートリアルでは、幾何異性についてすべて学びます .これは、異性体の概念の紹介から始まります。ここでは、さまざまなタイプの異性体を定義して説明します。次に、アルケンとシクロアルカンの両方の幾何異性を調べます。その過程で、幾何異性体の cis-trans 表記と E-Z 表記の違いについて学びます。
他の記事で取り上げるトピック
- 立体異性体とキラル中心
- 立体障害
- 有機化学における官能基
- アルケン
- 椅子の構造
- ニューマン プロジェクション
異性体とは?
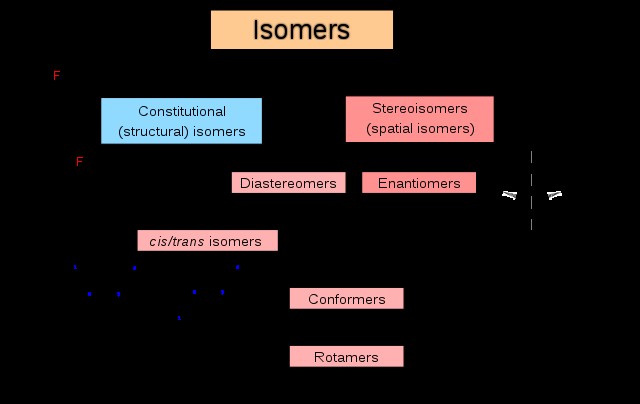
異性体は、同じ化学式を共有するが、原子の配置が異なる分子です。異性体には、構造異性体と立体異性体の 2 つの一般的なタイプがあります。構成異性体 (構造異性体とも呼ばれます) は、原子が互いに結合または結合する方法が異なりますが、立体異性体は原子の空間配置が異なります。
立体異性体は、鏡像異性体とジアステレオマーの 2 つのカテゴリにさらに分類できます。 エナンチオマー (光学異性体とも呼ばれます) は、重ね合わせることができない鏡像です お互いの。 ジアステレオマー 、一方、鏡像ではない立体異性体です お互いの。さらに、エナンチオマーは同一の化学的および物理的特性 (旋光度を除く) を持ちますが、ジアステレオマーはかなり異なる化学的および物理的特性 (沸点、溶解度、反応性など) を持つことができます。シス-トランス異性体と配座異性体 (すなわち配座異性体) は、特定の種類のジアステレオマーです。
幾何異性の紹介
シス-トランス異性としても知られる幾何異性は、立体異性の一形態です。すべての立体異性体と同様に、幾何異性体は、同じ構成原子で構成され、同じ順序で接続されているが、それらの原子の空間方向が異なる化合物です。
すべての幾何異性体は、官能基が化学結合の周りを自由に回転できないようにする分子内で制限された回転を必要とします。この制限された回転は、通常、炭素-炭素二重結合または環構造によって引き起こされます。
アルケンの幾何異性
炭素-炭素二重結合を含む化合物の幾何異性には、1 つの主要な要件があります。二重結合の各炭素原子は、2 つの異なる原子または官能基に結合する必要があります。
以下に示す例では、各二重結合炭素原子がメチル基と水素原子 (つまり、2 つの異なる基) に結合しているため、化合物の最初のペアがこの要件を満たしています。一方、2 番目の化合物ペアは、二重結合炭素原子の 1 つが 2 つの水素原子 (つまり、2 つの同一の基) に結合しているため、要件を満たしていません。
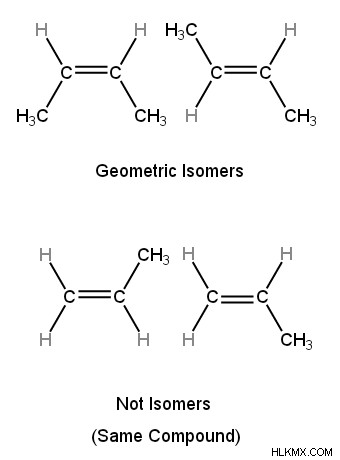
幾何異性体のシス-トランス表記法
ラテン語のプレフィックス cis とトランス それぞれ「のこちら側」と「の反対側」に翻訳されます。これらの線に沿って、シス異性体は二重結合の同じ側に官能基を持ち、トランス異性体は二重結合の反対側に官能基を持つことは理にかなっています.
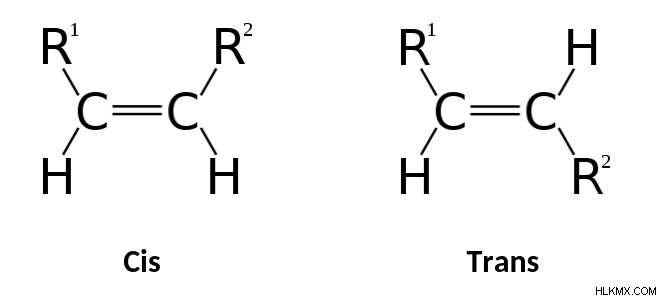
幾何異性体の E-Z 表記法
炭素-炭素二重結合は、一般に置換基 (水素以外の原子または基) の数に基づいて分類されます。アルケン置換パターンの例を以下に示します。
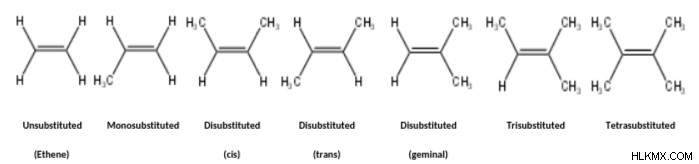
cisという用語は とトランス 二置換アルケンの幾何異性体を特定する場合に役立ちますが、3 つまたは 4 つの置換基を持つアルケンには適用されません。一方、E/Z システムは、二置換、三置換、および四置換アルケンに適用されます。
E/Z 命名システムを使用する場合、従うべき 2 つの重要な手順があります。
- ステップ 1:Cahn-Ingold-Prelog 規則を使用して、二重結合の両側で優先順位の高いグループを特定します。これらのルールについては、こちらで詳しく説明しています。
- ステップ 2:優先度の高い 2 つの基が炭素-炭素二重結合の同じ側にあるか反対側にあるかを判断し、E を割り当てます。 または Z
配置 Z の異性体 (ドイツ語の zusammen に由来) 、「一緒に」を意味する)は、二重結合の同じ側に優先順位の高い置換基を持っていますが、配置Eの異性体(ドイツ語のentgegenから) 、「反対」を意味する) は、二重結合の反対側に優先順位の高い置換基を持っています。
E/Z 命名システムを使用した幾何異性の 2 つの例を以下に示します。上記の手順に従って、各異性体に E が与えられます。 または Z
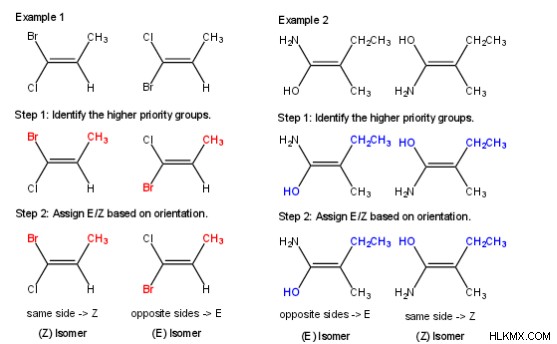
シクロアルカンの幾何異性
環状化合物を扱う場合、ウェッジとダッシュを使用して、環の置換基の相対的な方向を示します。くさびは環の平面の上の化学結合 (つまり、手前に来る) を表し、点線は環の平面の下の化学結合 (つまり、遠ざかる) を表します。
幾何異性は、二置換シクロアルカンで一般的に観察されます。シス異性体には、同じ向きの 2 つの置換基があります (2 つのくさびまたは 2 つの破線で示されます)。一方、トランス異性体には、反対方向の 2 つの置換基があります (1 つのくさびと 1 つの破線で示されます)。

シクロアルカンは、炭素-炭素二重結合の存在を必要とする E-Z 表記を使用しません。
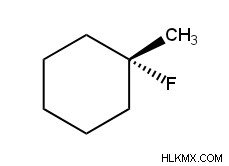
両方の官能基が同じ炭素に結合している場合、二置換シクロアルカンには幾何異性が適用されないことに注意することも重要です。たとえば、1-フルオロ-1-メチルシクロヘキサン (以下に示す) には幾何異性体がなく、シスまたはトランスの指定はありません。
さらに読む
- 共鳴構造
- カルボカチオン安定性
- Sn1 と Sn2 の反応
- E1 と E2 の反応を理解する