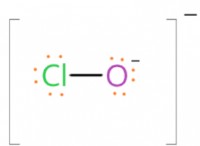その理由は次のとおりです。
* 安定性: 原子は、最も外側のシェル(価数シェル)がいっぱいになると最も安定しています。ほとんどの要素では、これは8つの原子価電子を持つことを意味します。
* イオン結合: 原子がイオンを形成すると、電子を獲得または失い、完全な価数シェルを達成します。
* カチオン(陽性イオン): 原子は電子を失い、陽イオンになり、原子価の電子が少なくなります。
* アニオン(負イオン): 原子は電子を獲得して陰イオンになり、より多くの価電子を与えます。
オクテットルールの例外:
* 水素とヘリウム: これらの要素には、安定性があるために、価数シェルに2つの電子のみが必要です。
* 3行目以下の要素: これらの元素は、d軌道が利用可能であるため、イオンに8つ以上の価電子を持つことがあります。
例:
* ナトリウム(Na): 1価電子が1つあります。この電子を失い、0価電子が0でna+になります。
* 塩素(cl): 7つの価電子があります。 1つの電子を獲得してCl-になり、8つの価電子を備えています。