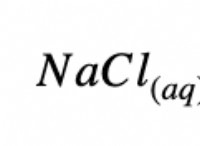何が水分極を作るのですか?
* 電子の不均一な共有: 水中の酸素原子は、水素原子よりも電気陰性です。つまり、共有電子をそれ自体に近づけます。これにより、酸素の近くに部分的な負電荷(Δ-)が生成され、水素の近くに部分的な正電荷(Δ+)が生成されます。
* 曲がった形: 水分子の形状は曲がっており、これはさらに不均一な電荷分布に寄与します。
水の極性の結果:
* 強い水素結合: 水素原子の部分的な正電荷は、他の水分子の酸素原子の部分的な負電荷を引き付け、強い水素結合を形成します。これらの結合は、多くの水のユニークな特性を担当しています。
* 優れた溶媒: 水の極性により、多くのイオン化合物と極性分子を溶解できます。これは、水中の部分的な電荷が溶質の反対の電荷と相互作用し、それらを引き離す可能性があるためです。
* 高融点と沸点: 水分子間の強い水素結合は、壊れるために多くのエネルギーを必要とし、同様のサイズの他の分子と比較して高い融点と沸点をもたらします。
* 高い表面張力: 水分子間の強い水素結合は、強い凝集力を生み出し、高い表面張力を引き起こします。これが、水が液滴を形成し、昆虫が水の上を歩くことができる理由です。
* 生物学的プロセスにとって重要: 水のユニークな特性は、生命に不可欠です。それは、生物学的反応の溶媒として機能し、栄養素を輸送し、温度を調節し、他の多くの重要なプロセスに参加します。
水が非極性の場合:
* 水素結合なし: 水は、この相互作用に必要な部分的な電荷が欠けているため、水素結合を形成しません。
* 溶媒が悪い: 水は多くのイオン化合物や極性分子を溶解することはできません。
* 融点と沸点の低い: 水は、融点と沸点がはるかに低く、おそらく室温でのガスでさえあります。
* 低表面張力: 水は、液滴を形成せず、昆虫を支えることができず、表面張力が非常に低くなります。
結論: 水の極性は、そのユニークな特性と人生における重要な役割に絶対に不可欠です。それが非極性の場合、それは非常に異なる特性を持つ非常に異なる物質になります。