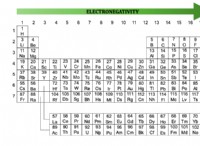
これは、反応性が金属にどのように現れるかの内訳です。
* 酸化: 金属は電子を簡単に失う傾向があり、積極的に帯電したイオンになります。このプロセスは酸化と呼ばれ、金属を含む多くの重要な化学反応の基礎です。
* 酸との反応: 多くの金属は酸と反応し、水素ガスと塩を生成します。金属と酸との反応性は、電子を失う能力の尺度です。
* 水との反応: 一部の金属は水と反応し、金属水酸化物を形成し、水素ガスを放出します。水と水との反応性は、反応性系列における金属の位置に依存します。
* 酸素との反応: 金属は酸素と反応して酸化物を形成します。この反応は室温で遅くなる可能性がありますが、熱または水分によって加速することができます。
* 他の要素との反応: 金属は、硫黄、ハロゲン、窒素などの他の元素と反応して、さまざまな化合物を形成することができます。
金属のその他の重要な化学的特性は次のとおりです。
* 電気伝導率: 金属は、電子を簡単に失う能力のため、電気の優れた導体です。
* 熱伝導率: 自由電子はエネルギーを簡単に伝達できるため、金属は熱の良好な導体です。
* Malleability: 金属は、壊れることなく薄いシートにぶつかったり、丸めたりすることができます。
* 延性: 金属はワイヤーに引き込むことができます。
金属の特定の化学的特性は、個々の金属によって異なることに注意することが重要です。たとえば、ナトリウムは非常に反応性が高く、水と激しく反応しますが、金は比較的反応性がなく、耐食性に耐性があります。