ルール:
* グループ番号(従来の番号付けシステムを使用)は、価電子電子の数に直接対応しています。
説明:
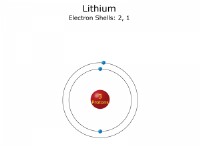
* 価電子 原子の最も外側のエネルギーレベルの電子です。これらは化学的結合に関与する電子です。
* グループ 周期表には垂直列があります。
* 従来の番号付け グループに左から右に1〜18に番号が付けられている古いシステムを指します。
例:
* グループ14(炭素グループ): このグループの元素には、4つの価電子があります。
* グループ17(ハロゲン): このグループの要素には、7つの価電子があります。
* グループ18(Nobleガス): このグループの元素には、8つの価電子があります(ヘリウムを除き、2があります)。
重要なメモ:
* このルールは、特にグループ13-18(メイングループ要素)に適用されます。 遷移金属には適用されません(グループ3-12)。
* ルールは、最も外側のエネルギーレベルの * s *および * p *軌道の電子の数に基づいています。
* グループ内の要素は、同様の化学的特性を共有しています 彼らは同じ数の原子価電子を持っているため、他の要素との結合方法に直接影響するからです。
より多くの例をご覧になりたい場合はお知らせください!