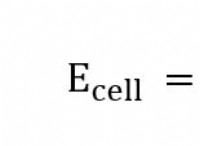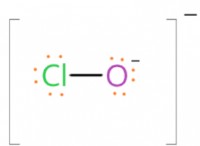料金の理解
* 硫黄 周期表のグループ16にあり、通常は-2の電荷があります。
* 金属 さまざまな料金がかかる可能性があり、この場合は「M」の料金を把握する必要があります。
料金のバランス
1。合計負電荷: 3つの硫黄原子があるため、合計負電荷は3 *(-2)=-6です。
2。総正電荷: -6電荷のバランスをとるには、2つの「m」原子の合計正電荷は+6でなければなりません。
3。 m原子あたりの電荷: したがって、各「M」原子の電荷は+6 / 2 =+3です。
結論
化合物の金属(m)の電荷m₂s₃は +3 です 。