グラフェンは、世界中の材料研究を変革しました。グラフェンは、さまざまな分野に影響を与える可能性のある革新的な素材と見なされています。グラフェンの電子的、化学的、および構造的側面は、その広範な応用の可能性を担っています。注目を集める炭素の同素体であるグラフェンは、二次元 (2D) クラスの材料に属します。
グラフェンの応用範囲が認識されたことで、実際に 2D 材料が普及し、研究者は新しい層状構造を発見するようになりました。グラフェンは、sp 混成炭素原子で形成された独特のハニカム構造を持っています [1]。その電気伝導性と熱抵抗により、グラフェンは電子デバイス、ストレージ アプリケーションなどに最適な選択肢となります。グラフェンのπ共役の可能性により、芳香族薬物の薬物送達が可能になります。特に、グラフェンは光熱療法で研究されています [2]。
グラフェンとともに、酸化グラフェン (GO) や還元型酸化グラフェン (rGO) などの他のグラフェン関連材料も関心を集めています。酸化グラフェンは、グラフェンが酸化された形です。さまざまな還元剤によるGOの還元により、元のグラフェンに匹敵する特性を持つrGOが得られます。グラファイトから得られたグラフェンと比較すると、rGOには欠陥があります。しかし、rGO を使用すると、グラフェンを低コストで大量に入手できます。したがって、rGO はさまざまなアプリケーションで広く調査されています。水和ヒドラジン、アスコルビン酸、NaBH4 などのさまざまな還元剤 などは、GO リダクション (3) に使用されます。ヒドラジン水和物のような有毒な還元剤を利用することは、爆発性があり使用が難しいため不利です.
一方、アスコルビン酸は、GOをrGOに効果的に還元できる穏やかな還元環境を提供します。アスコルビン酸でGOを還元して生成されたrGOは、元のグラフェンと同じくらい優れた特性を示しました。合成コストが低く、反応条件をより適切に制御できるため、アスコルビン酸は rGO 合成の理想的な還元剤になりました (4)。
rGOは、元のグラフェンと同じ電子特性を得ることを目的として合成されています。同時に、GO を rGO に還元すると、酸素官能基が減少するため疎水性が増加し、最終的に凝集につながります。水の安定性が低いと、生物医学的用途への適用性に影響します。 rGO表面を機能化することは、rGOの安定した水懸濁液を得る1つの方法であり、毒性を低下させ、生細胞との適合性を改善するという利点が追加されています(5)。ポリエチレングリコール (PEG)、デキストラン、ポリビニル アルコール、プルロニックなどの界面活性剤やポリマーは、機能化に広く使用されています。ポリ(エチレンオキシド)-ブロック-ポリ(プロピレンオキシド)-ブロック-ポリ-(エチレンオキシド)からなるプルロニック構造のトリブロック共重合体による表面官能化により、かなり安定したrGOの水分散液が得られます(6)。
GO の rGO へのアスコルビン酸還元とそれに続くプルロニクスを使用した機能化により、プルロニクスで安定化された rGO が 80% を超える収率で生成されました。 FT-IR、XRD、ラマン分光法、XPS、TGA、TEM、XPS などのさまざまな手法を使用して合成されたプルロニクス安定化 rGO の特性評価により、GO の rGO への還元の成功と、rGO 表面へのプルロニクスの効果的な結合が確認されました。物理化学的特性評価とは別に、ナノ粒子の生物学的特性評価も重要です。
エンドトキシン検出は、ナノ粒子の主要な生物学的特性評価手法です。エンドトキシンの干渉により誤った結果が生じる可能性があるため、ナノ粒子は生物学的アッセイの前にエンドトキシンフリーである必要があります。 rGO およびプルロニクスで安定化された rGO のエンドトキシン評価により、両方のナノ粒子のエンドトキシン限界が、医薬品および医療機器の USP 推奨エンドトキシン レベル (0.5 EU/ml) 未満であることが明らかになりました。したがって、rGO とプルロニクスで安定化された rGO の両方が、より徹底的な調査の後、生物医学的アプリケーションに推奨されます。
タンパク質のコロナ形成は、体内に投与された場合のナノ粒子の運命を決定し、重要な生物学的特性評価技術と見なされています (7)。タンパク質や生体分子はブロマン効果によってナノ粒子の表面に吸着し、硬いコロナと柔らかいコロナを形成します。形成されたタンパク質コロナは、ナノ粒子の循環、代謝、および排泄の生物学的反応を決定します。 rGOおよびプルロニクスで安定化されたナノ粒子のSDS分析により、rGOのタンパク質結合能力が高いことが明らかになりました。プルロニクスで安定化されたrGOでは特定のバンドは観察されず、タンパク質吸着が低いことを意味します。低いタンパク質吸着は、プルロニクスにおける PEG 部分の存在に起因する可能性があります。 PEG はタンパク質結合を低下させ、細網内皮系への浸透を可能にします (8)。
血液脳関門 (BBB) は、神経系を保護する重要な境界です。同時に、BBB はニューロン部位での薬物送達を妨げます。 BBB を通過するナノ粒子の能力により、ナノ粒子はさまざまな神経細胞アプリケーションで信頼できるものになります (図 1)。
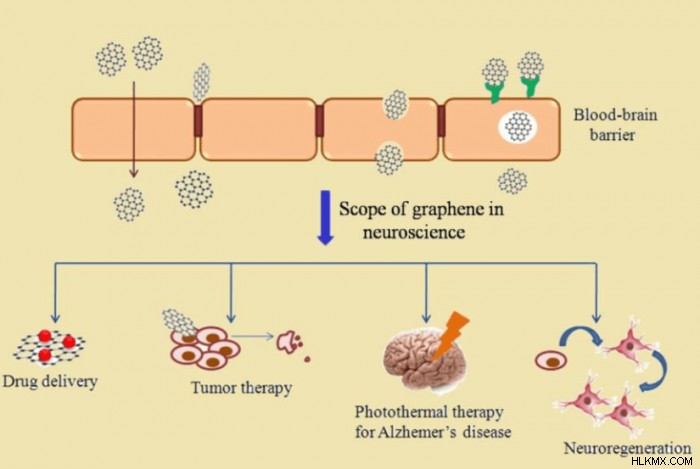
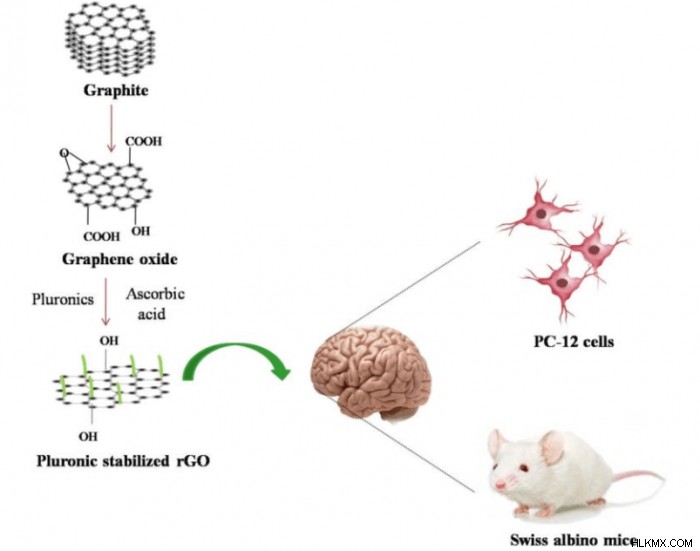
グラフェンは、文献によると、薬物送達、脳深部刺激、標的療法などに最適です (9)。魅力的なことに、グラフェンはアルツハイマー病の光熱治療の可能性について広く研究されてきました (10)。 BBB を通過する能力とは別に、グラフェンは幹細胞のニューロンへの増殖と分化を誘導することもできます。これは、ニューロン再生の基本的な特性です。生物医学的用途でグラフェンを使用する前に、グラフェンの生体適合性を検証する必要があります。 rGO、およびプルロニクスで安定化された rGO は、粒子による神経生理学的変化に対して安全であるとマークする必要があります。したがって、ラット褐色細胞腫細胞株である PC-12 細胞を選択して、rGO とプルロニクスで安定化した rGO の両方の効果を分析しました (図 2)。
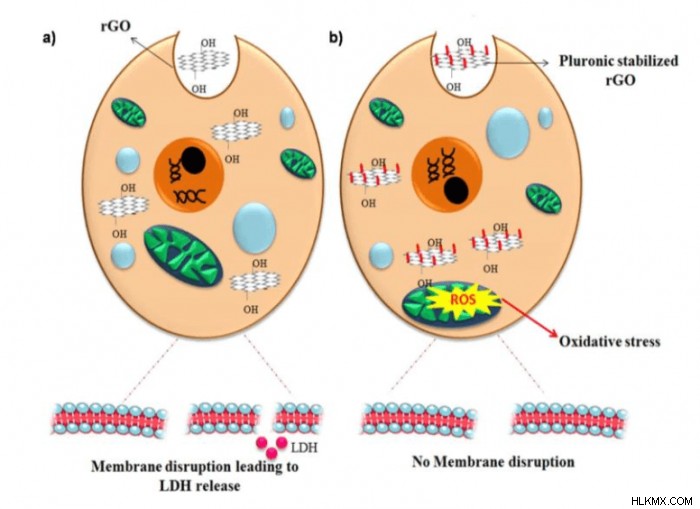
PC-12 には、神経成長因子 (NGF) に応答してニューロンを分化させる能力があります。 PC-12細胞をrGOおよびプルロニクスで安定化したrGOで処理した場合、MTSアッセイ分析は用量依存的な毒性を示しました。乳酸脱水素酵素(LDH)アッセイの結果によると、rGOはLDH放出の増加から明らかなように膜破壊を誘発しました。一方、プルロニクスで安定化されたrGOは、LDH放出の顕著な上昇を誘発しませんでした。したがって、プルロニクスの安定化により、rGO の膜破壊傾向が減少したと推測できます。
rGOおよびプルロニクスで安定化されたrGOで処理されたPC-12細胞の細胞骨格の完全性は、β-IIIチューブリン染色によって分析されました。 rGO は、高濃度で細胞骨格破壊を誘発しました。プルロニクスで安定化したrGOで処理した細胞では、明らかな細胞骨格の破壊は検出されませんでした。酸化ストレスは、ナノ粒子による毒性の主な原因です。
そのため、ナノ粒子によって誘発される ROS 生成は、関連する毒性について知るために監視する必要があります。 rGOは、PC-12細胞でのROS生成を支持しませんでした。 rGO の疎水性は、細胞との相互作用を制限します。これが、rGO 処理細胞での ROS 検出が低い理由である可能性があります。グラフェンのラジカル捕捉挙動は、ROS 生成の低減にも役立ちます (11)。プルロニック安定化rGOで処理されたPC-12細胞は、未処理の細胞と比較してより高い量のROSを示しました。プルロニック安定化 rGO のコロイド安定性は、用量濃度の増加に応じて ROS の増加を引き起こす、より優れた細胞相互作用を促進します (図 3)。
in vitro 以外 モデル、in vivo での rGO およびプルロニクス安定化 rGO の効果 レベルも分析した。 Swiss Albino マウスに、10mg/ml 濃度の rGO およびプルロニクスで安定化した rGO を、静脈内 (i.v) および腹腔内 (i.p) の両方の経路で投与しました。 rGO およびプルロニクスで安定化された rGO は、投与後 72 時間まで検出可能な毒性を誘発しませんでした。処置したマウスでは、行動の変化や体重減少は観察されませんでした.
結果は、プルロニクス安定化によって安定したrGO分散を得るための環境に優しく、信頼性が高く、低コストのルートを提唱しました。ナノ粒子はin vitroで用量依存的な毒性を示しましたが、 in vivo では実質的な毒性は検出されませんでした。 レベル。提案された材料は、生物医学的応用におけるその範囲をより明確に把握するために、繰り返し曝露するためにさらに調査する必要があります.







