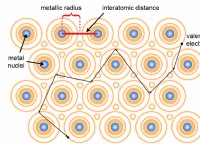
これが故障です:
* 温度: 粒子の平均速度は、物質の温度に直接関連しています。 温度が高いほど、平均速度が速くなります。
* 分子量: 重い粒子(高分子腫瘤)は、同じ温度で軽い粒子よりも遅く移動します。
* 物質状態: 液体の粒子よりもゆっくりと動く固体の粒子は、ガス内の粒子よりも遅く移動します。
粒子速度をよりよく理解するために、ここにいくつかの重要な概念があります:
* ルート平均速度(VRMS): これは、粒子の平均速度を表現する一般的な方法です。これは、すべての粒子の平方速度の平均の平方根として計算されます。
* 最も可能性の高い速度: これは、粒子の最大数が動いている速度です。
* 平均速度: これは、すべての粒子の速度の算術平均です。
式:
* vrms =√(3kt/m) 、 どこ:
* kはボルツマン定数(1.38 x 10^-23 j/k)です
* Tはケルビンの絶対温度です
* mはkgの1つの粒子の質量です
例:
室温(298 K)で窒素分子(N2)のガスがあるとしましょう。 VRMSの式を使用して、計算できます。
* vrms =√(3 * 1.38 x 10^-23 j/k * 298 k/(28 x 1.66 x 10^-27 kg))≈515m/s
これは、室温での窒素分子の平均速度が毎秒約515メートルであることを意味します。
覚えておいてください: Maxwell-Boltzmannの分布は、平均速度だけでなく、速度の範囲があることを示しています。一部の粒子ははるかに遅く動きますが、他の粒子ははるかに速く動きます。