その理由は次のとおりです。
* 主要な量子数(n): 主要な量子数は、電子のエネルギーレベルを説明しています。 n =3は3番目のエネルギーレベルに対応します。
* 角運動量量子数(l): 角運動量量子数は、軌道の形状を表します。 0〜N-1の範囲です。 n =3の場合、Lの可能な値は0、1、および2です。これらは以下に対応しています。
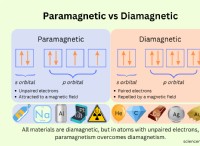
* l =0:s軌道(球状)
* l =1:p軌道(ダンベル形状)
* L =2:D軌道(より複雑な形状)
n =3にはl =3がないため、3f軌道はありません。
より高いエネルギーレベルについて考えている場合、F軌道の最初の外観はn =4(4f軌道)です。