コア コンセプト
この記事では、酸を構成するものの基本的な定義と、酸の命名規則について学びます。 .また、強酸と弱酸が水中でどのように解離するかについても学びます。
他の記事で取り上げるトピック
- KSP – 溶解度積定数
- 一塩基性、三塩基性、および多塩基性酸
- 溶解度とは?
- 溶解度のルールとチャート
- 平衡定数とは?
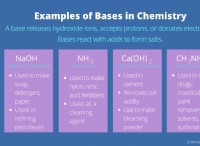
酸とは?
酸は、プロトンを供与できる分子またはイオンであり、ブレンステッド・ローリー酸として知られています。酸は、ルイス酸として知られる電子対と共有結合を形成する分子として定義することもできます。酸は常にイオンまたは分子になります。酸はどのように分子ですか.さて、すべての酸は非金属で構成されており、分子は共有結合の別名にすぎません.水素イオン (水素にはプロトンが 1 つしか含まれていないため、プロトンとも呼ばれます) は、酸の重要な要素です。酸を特定するもう 1 つの良い方法は、化学式で (aq) 記号を探すことです。これは、溶液が水性であることを示します。つまり、水に溶けます。水性になる種の 1 つが H である場合、それは酸の指標です。
私たちのほとんどは以前に酸について聞いたことがありますが、酸が強いか弱いかを分類するものは何ですか?水素原子が完全に解離するか、部分的にしか解離しないかによって、酸が強いか弱いかが決まります。これは、強酸の場合、酸をビーカーの水に入れると、水素イオンが溶液中の元の分子から 100% 離れた状態で検出されることを意味します。強酸は、硫酸、硝酸、塩酸、臭化水素酸、ヨウ化水素酸、過塩素酸の 6 つだけです。
例として、HCl (塩酸) と HF (フッ化水素酸) を使用しましょう。
塩酸の化学式:HCl(aq) → H(aq) + Cl(aq)

フッ化水素酸の化学式:HF(aq) ⇄ H(aq) + F(aq)

化学式に基づくと、HCl は強酸であるため、完全に解離します。ただし、フッ化物イオンと水素イオンだけでなく、溶液中に無傷の HF が存在するため、HF の式には平衡矢印があります。 HF は水分子に付着し、溶液を塩基性にするヒドロニウムを形成します。
酸の名前の付け方
酸素による酸の命名
第 1 の硝酸の例-
- まず – 多原子陰イオンを特定します Hいいえ3 → いいえ3 これが硝酸塩であることを認識してください
- 二番目 – 多原子イオン NO3 の名前を書きなさい =硝酸塩
- 3 番目 – 接尾辞 -ate を -ic Nitrate に変更します → 硝酸
- 4 番目 – 名前に酸という単語を追加 (硝酸)
例 2 の亜硫酸-
- まず – 多原子陰イオンを特定します HSO3 → SO3 これが亜硫酸塩であることを認識してください
- 2 番目 – 多原子イオン SO3 の名前を書きます =亜硫酸塩
- 3 番目 – 接尾辞 -ite を -ous 亜硫酸塩 に変更します →硫黄
- 4 つ目 – 名前に酸という単語を追加する (亜硫酸)
(リン酸の綴りもリン酸に変わりますor ic酸を使用するとより良い音になります)
酸素を含む酸にはそれらの多原子陰イオンが含まれているため、一般的な多原子イオンのリストを覚えておくことをお勧めします。

酸素を含む酸の命名規則を要約すると、-ate で終わる多原子陰イオンは -ic 酸になります。 -ite で終わる多原子陰イオンは -ous 酸になります
酸と酸素の化学式を書く
第 1 の塩素酸の例-
- まず – 水素陽イオンの記号 – H を書きます =水素イオン
- 2 つ目 – 接尾辞 -ic を接尾辞 -ate Chloric に置き換えて、酸の名前の多原子陰イオンを特定します。 酸 → 塩素酸塩
- 3 番目 – 多原子陰イオン塩素酸 =ClO3 の化学式を書きます
- 4 つ目 – 水素カチオンの化学式を組み合わせます 多原子陰イオン HとClO3 1:1 の比率 1(+1) + 1(-1) =0 を持ちます。これは、化合物が中性 HClO3 であることを意味します
- 5 つ目 – 下付き文字 (aq) を書いて、その物質が水溶液であることを確認します。
酸素を含まない酸の命名
第 1 の HCl の例 –
- まず – 単原子陰イオン HCl → Cl を特定します
- 2 番目 – 単原子陰イオン Cl =塩化物の名前を書きます
- 3 番目 – 単原子アニオンの接尾辞 -ide を -ic に置き換えます。塩化物→塩素
- 4 番目 – プレフィックス Hydro を追加します Acid という単語 .したがって、塩酸が得られます
例その 2 H2 S –
- まず – 単原子陰イオン H2 を特定します S→S
- 2 番目 – 単原子アニオン S =スルフィドの名前を書きます
- 3 番目 – 単原子アニオンの接尾辞 -ide を -ic に置き換えます。 Sulfide → Sulfuric (発音を良くするためにスペルが少し変更されています)。
- 4 番目 – プレフィックス Hydro を追加します Acid という単語 .したがって、硫酸水素塩が得られます
(りんのつづりもりんに変わります)
酸素を含まない酸の命名規則を要約すると、酸素を含まない酸の化学名は常に接頭辞 -hydro で始まり、接尾辞 -ic で終わります。