コア コンセプト – 結合長
このチュートリアルでは、化学結合の定義と、結合順序の主な違いについて学習します。 r と 結合長 .また、これらの特性が互いにどのように関連しているかを学び、それらを化学構造に適用できるようにします。
他の記事でカバー
- イオン結合
- 共有結合
- 金属結合
- 水素結合
- 共鳴構造
語彙
共有結合: 2 つの原子 (通常は非金属) 間の電子の共有による原子結合。
分子: 2 つ以上の原子が結合して形成される化合物。
債券とは
化学結合は、化合物の形成を可能にする分子または原子間の力です。結合は、原子間に存在する引力から生じます。
債券注文とは?
結合順序は、一対の原子間に存在する共有結合の数です。また、結合次数が高いほど結合が安定していることを示すため、結合の安定性を判断するためにも使用されます。これは、電子間の引力が増加し、分子内の原子がより緊密に結合されるためです。
債券の順序を決定する手順:
2 つの原子間の結合順序:
<オール>例:

水酸化物では水素原子と酸素原子の間に単結合があるため、全結合次数は 1 です。
多原子分子の結合順序:
<オール>例:

硝酸塩の酸素原子と窒素の間に合計 4 つの結合があるため、結合基が 3 つ存在するため、合計の結合順序は 4/3 です。
結合長とは?
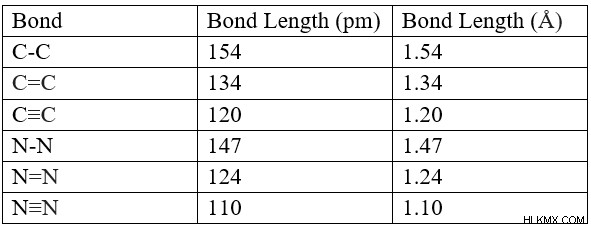
結合長は、結合した原子の核間の距離を表します。結合の長さは結合次数に反比例します。結合次数が高いほど、結合の長さが短くなります。これは、結合次数が高くなると原子間の引力が増加し、結合が短くなるために発生します。結合長は pm (1 ピコメートル → 10 メートル)、または Å (1 オングストローム→10 メートル) で測定されます。
結合長の例: