コア コンセプト
この有機化学のチュートリアルでは、アルキンの構造、反応、簡単な事実、注目すべき例など、アルキンについて学びます。
アルキンの構造
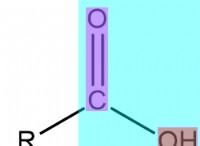
化学者は、「アルキン」という用語を使用して、炭素-炭素三重結合を持つ有機化合物を指します。炭化水素では、この三重結合が主要な官能基として機能します。この三重結合には、1 つの非反応性のシグマ結合と 2 つの反応性のパイ結合があります。
アルキンの一般式は RCΞCR' です。アルキンの炭素には、三重結合とそれぞれの可変基の 2 つの電子ドメインしかないため、sp があります。 ハイブリダイゼーション。エチンは、式 HCΞCH:
の最も単純なアルキン構造を持っています。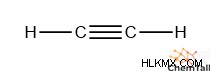
アルケンの概要
- 構造:別の炭素に三重結合した炭素。

- 一般式:Cn H2n-2 、ここで n ≥ 2
- 酸性度:アルケンやアルカンよりも酸性
- 溶解度:水には不溶ですが、ジエチル エーテルなどの非極性有機溶媒には溶けます
- CΞC 結合長:1.21 Å
- CΞC 結合エンタルピー:812 kJ mol-1 IR分光法:アルキン三重結合(CΞC)は、一置換か二置換かに応じて、2140〜2260cmでピークを形成する。 Csp – 末端アルケンの H 結合は、3267 ~ 3333 cm にピークを形成します。
末端アルキン
水素がアルキン官能基に結合すると、化学者はその結果生じる基を「末端アルキン」と呼びます。これは、そのような基が炭化水素の末端に位置するためです。この種類のアルケンは、その結合水素が非常に酸性であるため、特別です。
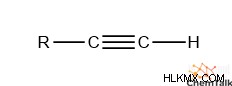
一般に、炭素に結合した水素は、C-H 結合が強いため、酸性度が非常に低くなる傾向があります。アルドール縮合に重要な、カルボニルに隣接する炭素に結合した水素など、いくつかの例外があります。末端アルキン水素は が高いため、この傾向を打ち破ります。 sp の特徴 C-H結合。
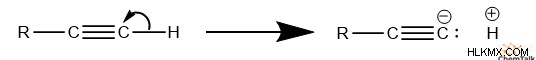
この酸性度により、十分に強い塩基と相互作用すると、末端アルキンの水素が解離します。末端アルキンは、その後の反応で求核剤として機能できるカルバニオンになります。
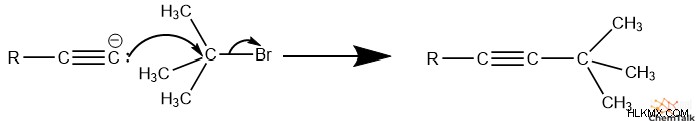
アルキンの例
アルキンは、アルケンと同等の、よく知られた命名規則に従います。アルキンを持ち、他の官能基を持たない炭化水素の場合、化合物の名前はアルキンの位置の最小数の炭素であり、その後に化合物内の炭素数を示す接頭辞 (eth-、prop-、but- など) が続きます。 .)、最後に接尾辞 -yne.
たとえば、1 つの末端アルキンを持つ炭化水素間では、最初の 10 個の化合物名には以下が含まれます:
- エチン
- プロピン
- 1-ブチン

- 1-ペンチン
- 1-ヘキシン
- 1-ヘプチン
- 1-オクチン
- 1-ノニン

- 1-デシン
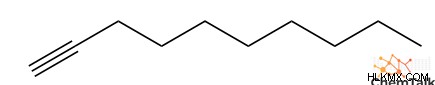
- 1-ウンデシン
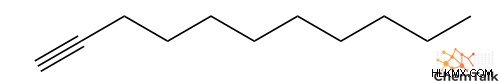
他の官能基やより複雑な命名法を持つ化合物の場合、アルキンはアルケンの等価物と同じ規則に従います:

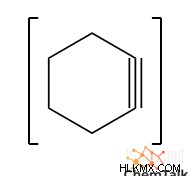
ご覧のとおり、多くのアルケン分子には安定したアルキン等価物もあります。これに対する 1 つの例外は、シクロアルケンです。「シクロアルキン」は、通常は直鎖の CΞC 結合の耐え難い環ひずみのために、形成されるのと同じ速さで分解する傾向があるためです。
アルキンとの反応
アルキンは、三重結合ではなく炭素-炭素二重結合を含むアルケンと同様に動作します。末端アルキンの酸性度は別として、アルキンは本質的に二重アルケンのように振る舞い、同じ炭素対に 2 つの反応性パイ結合があります。
アルキンとの付加反応
アルケンと同様に、特定の求核求電子化合物は、各アルキン pi 結合で付加反応を実行できます。たとえば、アルキンと HCl の付加反応を見てみましょう。
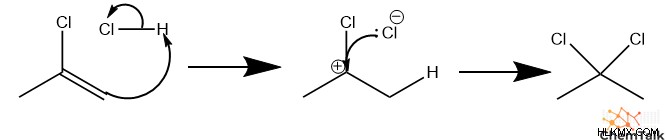
この例では、プロピンを使用しましょう。最初に、HCl はアルキンをプロトン化し、パイ電子のペアの 1 つを使用して C-H 結合を形成します。得られた分子はビニルカチオンであり、化学者がアルケン炭素に正電荷を持つカチオンを表すために使用する用語です。ほとんどのカルボカチオンと同様に、ビニルカルボカチオンは、一次炭素 (C1) よりも二次炭素 (C2) に正電荷を配置することを好みます。この場合の「二次」は、1 つの非水素のみに結合した「一次」炭素とは対照的に、2 つの非水素に結合した炭素を表します。
次に、塩化物アニオンがカルボカチオンを攻撃し、ハロゲン化アルケン分子を形成します。
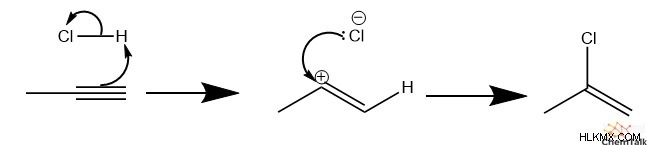
プロピル分子にはまだパイ結合があるため、過剰の HCl でさらに反応します。第三に、別の HCl がアルケンをプロトン化し、再び C2 にカルボカチオンを形成します。この場合、カルボカチオンは、塩化物の電子吸引効果によってさらに安定化されます。最後に、2 番目の塩化物がカルボカチオンを攻撃し、2,2-ジクロロプロパンを形成します。
アルキンの水和
上記のメカニズムはほとんどのアルキン付加反応に適用されますが、いくつかの例外が存在します。最も重要な例外は、アルキンへの水の付加です。再びプロピンを使用して、メカニズムを見てみましょう.
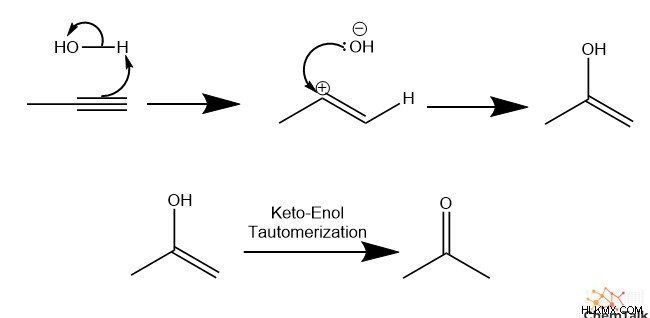
まず、HCl と同様に、最初の pi 結合がプロトン化され、結果として生じる水酸化物が 2 番目のビニル カルボカチオンを攻撃します。得られた化合物は、アルケン炭素にアルコールが結合した、化学者がエノールと呼ぶものです。エノール分子は安定性が低い傾向があります。次に、2 番目の追加を実行するのではなく、エノールはケト - エノール互変異性化を受けて、ケトンを形成します。
アルキンによるオゾン分解
アルケンと同様に、オゾンはオゾン分解によってアルキンと反応し、水性条件下でカルボン酸を形成します。末端アルキンはオゾン分解を行うことができないため、今回は 2-ペンチンでメカニズムを見てみましょう。
第一に、オゾンはアルキンに対して付加環化を実行し、ベンゼンのような電子の循環運動を伴います。これにより環状オゾニド化合物が形成される。第二に、電子の別の循環運動が発生し、環構造が壊れて、イオン性カルボニル オキサイド グループが形成されます。
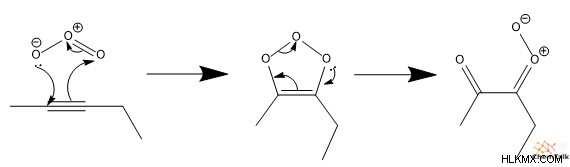
第三に、酸化カルボニルが水性環境からの水と反応し、最終的に 2 つのカルボン酸分子が生成されます。興味深いことに、ご覧のとおり、オゾン分解は炭素-炭素三重結合を完全に切断します。
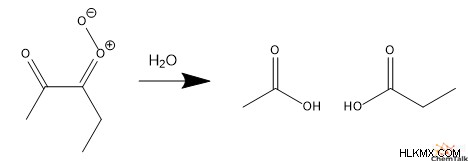
合成では、アルキンはカルボン酸よりも合成の汎用性が高いため、オゾン分解はほとんど使用されない傾向があります。ただし、化学者はオゾン分解を使用して、得られたカルボン酸フラグメントを分析することにより、未知のアルキンを分析します。