コア コンセプト
このチュートリアルでは、炭化水素、その構造、およびそれらに関連する有機化学反応について学びます。
炭化水素とは?
炭化水素は、炭素原子と水素原子のみを含む化合物の一種です。この単純さにもかかわらず、炭化水素は信じられないほど多様な化合物のグループです。炭化水素には 3 種類あり、それぞれに固有の共通の特徴があります。これらは、アルカン、アルケン、およびアルキンです。
炭化水素の命名
3種類の炭化水素はすべて同じ命名スキームを持っています。炭化水素の名前の接頭辞は、1 本の鎖に含まれる炭素原子の最大数に由来します。名前の 2 番目の部分は、化合物に含まれる結合の種類によって異なります。単結合しかない場合、名前には接尾辞 -ane が付きます。二重結合がある場合、名前には -ene サフィックスが付きます。三重結合の場合、名前には接尾辞 -yne が付きます。
プレフィックス
以下は、一般的な炭化水素プレフィックスの一部です:
| 炭素数 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| プレフィックス | 覚醒剤 | Eth | 小道具 | でも | ペント | 16 進数 | ヘプト | 10月 |
炭化水素の分岐
長い炭化水素鎖に結合する短い炭化水素鎖は、アルキル基、分岐、または置換基と呼ばれます。炭化水素に名前を付ける場合、分岐は主鎖のどの炭素に結合しているかによって番号が付けられ、その炭素数に対応する接頭辞が付けられます。
同じ置換基が複数回出現する場合、主鎖上の各位置に番号が付けられ、出現回数を示す別の接頭辞が追加されます。
炭化水素分子の立体化学
R と S の構成
立体化学の決定は、炭化水素の分類と命名の重要な部分です。炭素に 4 つの異なる基が結合している場合、それは立体中心と呼ばれます。ステレオセンターは、周囲のグループがどのように配置されているかに応じて、R または S ラベルを受け取ります。 R または S 構成を決定する最初のステップは、優先順位に従ってグループにラベルを付けることです。炭化水素の場合、立体中心のグループは、そのサイズに基づいて 1 から 4 までの番号を受け取ります。より大きなグループにはより低い数字が割り当てられ、水素には常に 1 が割り当てられます。
優先順位が最も低いグループは、後ろ向きで破線の結合にある必要があります。次に、グループ 1 からグループ 3 で終わる立体中心の周りに円形の矢印を描く必要があります。矢印が時計回りの場合、立体中心は R 配置になります。反時計回りの場合、ステレオセンターは S 構成になります。 R または S は、化合物名の残りの部分の前に括弧で囲みます。
2 つのグループの炭素数が同じであるが、グループの 1 つに二重結合または三重結合がある場合、より多くの結合を持つグループが優先されます。
アルケンの立体化学
アルケンには、命名時に立体化学的な考慮事項もあります。内部アルケンは、Z 配置または E 配置のいずれかになります。アルケンが E か Z かを判断するには、アルケン結合の方向に伸びる線を想像すると便利です。優先グループがこの線の同じ側にある場合、アルケンは Z です。優先グループが線の反対側にある場合、アルケンは E です。
アルケンでは、優先グループは、主鎖を構成する 2 つのグループです。

環状炭化水素
環状炭化水素は、名前の残りの部分の前に接頭辞「シクロ」を受け取ります。
炭化水素分子と名前の例
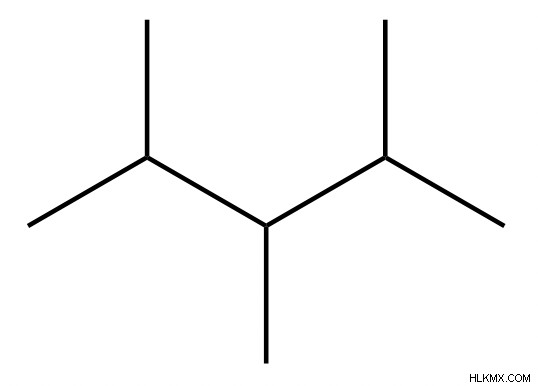
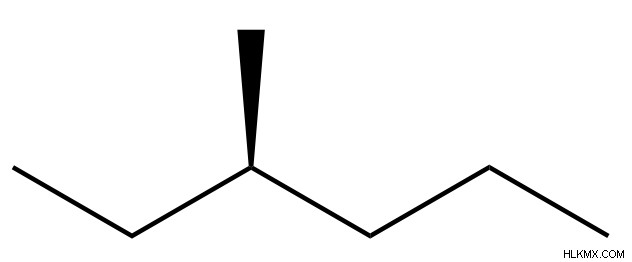
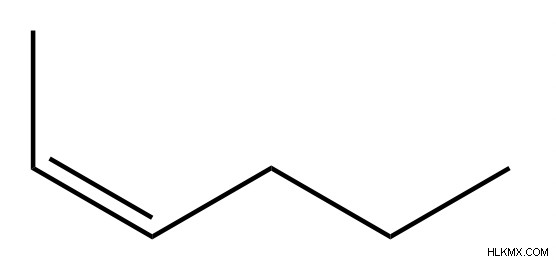
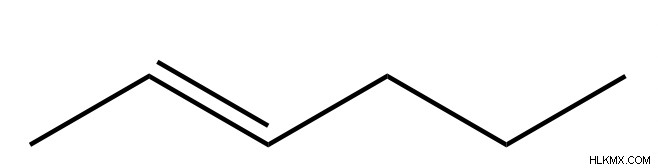
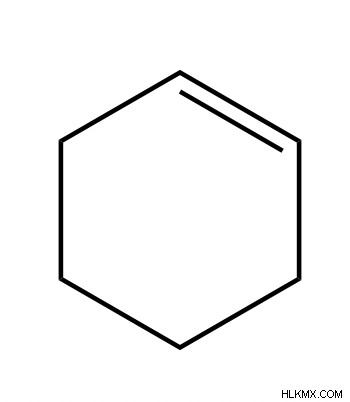
炭化水素の特性
膨大な数の炭化水素にもかかわらず、それらはすべて多くの特性を共有しています。極性がないため、炭化水素が経験する唯一の分子間力はロンドン分散力です。
さらに、炭化水素の沸点と融点は、炭素数とともに上昇します。分岐は、充填効率を下げることによって凝固点と沸点を下げます。これは、領域内の化合物がどれだけ密集しているかを示します。 2,3-ジメチルヘキサンとオクタンは同じ数の炭素原子と水素原子を持っていますが、オクタンは分岐していないため沸点が高くなります.
すべての炭化水素は可燃性です。それらは酸素との燃焼反応を行い、二酸化炭素、水蒸気、および熱を生成します。
最小の炭化水素であるメタンは、温室効果ガスです。これは、大気中に大量に集まると、太陽からの熱エネルギーを閉じ込めることを意味します.
炭化水素の用途
あらゆるタイプの炭化水素は、産業用および日常使用の両方で多様な機能を果たします。これらの用途の多くは、化石燃料産業の一部または直接的な派生物です。
燃料
自動車、トラック、飛行機などの内燃機関を搭載した車両は、炭化水素を燃料として使用します。これらの燃料は通常、単一の化合物ではなく、同じようなサイズの炭化水素の混合物です。大型車はより大きな燃料を使用する傾向があります.
炭素数 18 ~ 50 の鎖長を持つ炭化水素はモーター オイルとして使用され、エンジンを潤滑し、エンジンをスムーズに作動させます。
プラスチック
すべてのプラスチックが炭化水素であるわけではありませんが、多くの一般的なプラスチックが炭化水素です。一般に発泡スチロールとして知られているポリスチレンは、長鎖に重合されたスチレンで構成されています。プロピレンとポリエチレンの重合により、包装に使用されるプラスチックも生成されます。
溶剤
世界中の研究室で、化学者は炭化水素を非極性溶媒として使用しています。ヘキサンとトルエンは、有機実験室でよく使われる 2 つの溶媒です。過去の化学者は溶媒としてベンゼンをよく使用していましたが、現在では大量に使用するには発がん性が高すぎると考えられています.
リアクション
アルカン
アルカンは、最も少ない種類の反応に参加します。酸素にさらされると、アルカンは燃焼して CO2 を生成します 、水蒸気、および熱。さらに、アルカンはハロゲン化反応を受ける可能性があります。これらには、水素原子のハロゲンによる置換が含まれます。アルカンは、金属触媒の助けを借りて分解および結合することもできます.
アルケン
反応に関しては、アルケンはより多くの能力を持っています。ハロゲン化物分子とハロゲン化水素は、二重結合に付加してハロゲン化アルキルを形成します。同様に、水素分子は金属触媒の助けを借りて二重結合を水和することができます.
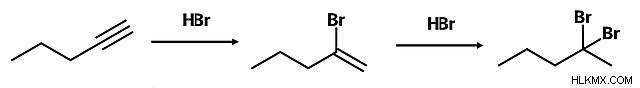
酸の存在下で水またはアルコールを追加すると、それぞれ -OH 基またはエーテルがアルケンに追加されます。
通常、これらの追加はマルコフニコフの法則に従います。これは、水素がアルケンの置換されていない側に追加されることを意味します。ボランとエーテル溶媒に続いて、塩基、水、過酸化水素を使用すると、水素の代わりに-OH基が置換の少ない側に追加されます.
オゾンとそれに続く還元剤は、アルケンを完全に二重結合で分解します。アルケンが末端の場合、これにより 2 つのアルデヒドが生成されます。アルケンが内部にある場合、これにより 2 つのケトンが作成されます。オゾンの後に酸化剤が続くと、結果は 2 つの酸になります。
アルキン
アルキンはアルケンと同様に反応します。 2 つの主な違いは、アルケンに付加するとアルカンが作成され、アルキンに付加するとアルケンが作成されることです。