この有機分子の存在は、さまざまな野菜や植物で観察できます。縮合式 HOOC-COOH のジカルボン酸で、ジカルボン酸の中で最も単純で、酢酸よりも強い酸強度を持っています。シュウ酸の過剰摂取は、健康に害を及ぼす可能性があります。それは、体内の炭水化物の酸化の結果として作成されます。この化合物の合成バージョンは、五酸化バナジウムなどの触媒の存在下、硝酸の存在下でスクロースを酸化することによって、実験室で作成することもできます.
シュウ酸は 2 つの多形構造で構成されており、最初の構造は白色の結晶性固体であり、水に溶解すると無色の溶液に変化します。共役塩基として機能するシュウ酸塩と組み合わせると、キレート剤としても使用できる還元剤です。
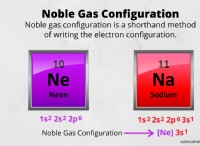
シュウ酸の式
シュウ酸は、食品加工で使用される分子式 C2H2O4 のジカルボン酸です。シュウ酸は、植物種 Oxalis と Rumex の細胞液に、それぞれカリウム塩とカルシウム塩の形で含まれています。
シュウ酸は弱酸で、水溶液中に存在すると部分的にしかイオン化しません。シュウ酸には、酸性の陽子が 2 つあります。最初のイオン化により、最終的にイオン化する弱酸である HC2O4– が形成されます。
シュウ酸は、利用可能な最も強力な有機酸の 1 つであり、炭酸やその他のさまざまな酸をその塩から溶解することができます。シュウ酸は、自然環境に見られる大部分の有機分子に対するカリの水和物または硝酸の作用によって形成されます。一部のサークルではジプロトン酸と呼ばれています。
シュウ酸の構造

シュウ酸が無水状態にある場合、シュウ酸は 2 つの異なる多形体で存在することに注意する必要があります。シュウ酸が最初の多形に変換されると、水素結合が発生します。この水素結合により、分子間レベルで鎖状構造を生成することが可能です。この化学物質の 2 番目の多形体が水素結合を受けている可能性もあります。しかし、この特定のシナリオでは、水素結合により、分子のシート状構造に似た分子間構造が生じます。この化学物質の 2 つの重要な特性のため、エステル化反応で一般的に使用されます。シュウ酸の酸性の性質は、エステル化プロセスに優れた選択肢となる最初の特徴です。シュウ酸の親水性は、この化合物の 2 番目で最も重要な特性です。
シュウ酸の調製
シュウ酸は、濃硝酸溶液の存在下でスクロースなどの特定の炭水化物を酸化することで簡単に作ることができます。シュウ酸は、酸化プロセス中に炭素原子が対になって引き裂かれるときに形成されます.
用途
- 染色工程で媒染剤として使用
- サビ取りに使用
- ランタニド化学における重要な試薬であり、他の多くの分野でも利用されています
- 大理石像を輝かせるために磨くのに使われます
- 染料の製造や漂白剤の製造に使用
- 食べ物やインクの染みの除去に使用
- 写真フィルムの現像に使用
- 時間の経過とともに蓄積したカルシウム沈着物を除去するために廃水処理に使用されます
健康被害
シュウ酸は毒物です。嘔吐、下痢、および重度の胃腸障害は、摂取に起因する可能性のある危険な症状の 1 つです。その他の症状には、腎障害、ショック、痙攣、昏睡などがあります。心血管虚脱は、死に至る可能性があります。シュウ酸は皮膚刺激物質であり、目、粘膜、および皮膚の刺激を引き起こす可能性があります.吸入または摂取の結果、腎臓障害が発生する可能性があります。
シュウ酸は毒物です。腎臓の損傷、ショック、および痙攣は、危険な副作用の一部です。毒性は、シュウ酸が組織内のカルシウムと反応してシュウ酸カルシウムを生成することによって引き起こされ、これによりカルシウム カリウム比のバランスが崩れます。尿細管にシュウ酸塩が蓄積すると、腎障害を引き起こす可能性があります。
シュウ酸の過剰摂取により、頭痛、めまい、吐き気、嘔吐、けいれん、昏睡、さらには死に至ることもあります。化学物質への過剰または繰り返しの曝露は、他の症状の中でも、皮膚の発疹、痛み、発赤、水ぶくれ、治癒の遅い潰瘍を引き起こす可能性があります.
結論
シュウ酸は、葉物野菜、レンズ豆、その他の植物性食品の大部分に含まれています。それは自然に発生する分子であるため、食事から摂取します。また、老廃物として体外に排出されます。シュウ酸塩が豊富な食品には、最適な健康のために体が必要とするさまざまな追加の栄養素も含まれています.
シュウ酸を含む食事を摂取すると、化学物質がミネラルに付着し、ミネラルが結合して追加のミネラルを形成します.シュウ酸鉄とシュウ酸カルシウムがそのような化合物の例です。
シュウ酸塩の少ない食事は、体内のシュウ酸塩のレベルが高いために腎臓結石が生成されるリスクが高い場合に有益です。ブロッコリー、チーズ、骨付き魚の缶詰などがその例です。また、かなりの量のカルシウムも含まれています。