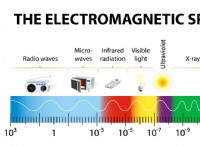
ハロゲン化は、1 つ以上の水素原子がハロゲン基に置き換えられる化学反応です。ハロゲン化合物の反応性の順番を見ると、フッ素>塩素>臭素>ヨウ素の順であり、フッ素は他の化合物よりも反応性が高いです。同時に、より攻撃的であるため、有機物質とのより多くの反応にも参加します。同時に、有機ハロゲンを最も安定にするのにも役立ちます。フッ素原子を反応させると、分離が非常に困難になることがあります。
同様に、ヨウ素が有機分子と反応しなければならない場合、ヨウ素をヨウ素有機にすることは非常に困難です。しかし、ヨウ素は反応後に簡単に除去できます。これに加えて、ハロゲン反応の原動力となるハロゲン原子の電気陰性度もわかります。この間、分子の性質も反応の完了に大きな役割を果たします。飽和炭化水素と不飽和有機ハロゲン化反応が起こる基質に応じて、いくつかのタイプのハロゲン化があります。
C6H6 + Cl2 → C6H5Cl + HCl
ハロゲン反応はなぜ重要なのですか?
化学合成はハロゲン反応にとって非常に重要であり、ハロゲン反応によって生成された製品は、医薬品、ポリマー、プラスチック、冷媒、燃料添加剤、難燃剤、農産物などの多くの場所で使用されていますフッ素のような要素が主ですまたは塩素は、医学などの主要分野でより良い治療のために使用されます.また、有機臭化物やオルガノジンなどの化合物の生成にも重要な役割を果たします。
基質として、化学は多くの分野で有用であることが証明されており、官能基の改善を助け、複雑な化学反応の基礎を提供しています。このアルコールは、反応中に加水分解されるのを助け、そこで C–Cl または C–Br 結合を形成するのに役立ちます。ケトン、アルデヒド、酸の形成を助ける酸化反応に役立ちます。
また、二重結合が形成される脱離反応にも不可欠です。化学反応中の有機化合物の臭素化は、しばしばグリニャール試薬の形成に役立ちます。同時に、ハロゲン化アルキルが試薬として使用されるフリーデル クラフツ反応中に主に必要とされる環のアルキル化にも役立ちます。さらに、フルオロエチレンをクロロジフルオロメタンに変換する際に主要な役割を果たします。
ハロゲン化反応の種類
ハロゲン化反応は、有機的および無機的の両方で行うことができ、基質が主な基礎を提供します。ここでは、ハロゲン化の方法について説明します。
- 飽和炭化水素によるフリーラジカル システム
- 不飽和生物のように
- 求電子置換のように
フリーラジカルハロゲン化またはハロゲン置換 - 飽和炭化水素は主に水素原子を使用し、水素原子は反応中にハロゲンに置き換えられます。ここでは、C–H 結合の相対的な弱さが反応で観察され、アルカンのハロゲン位置化学がこの反応で決定されます。この間、アルケンと反応してハロゲン化アルキルを生成しますが、熱が主な原因です。この反応の主な用途は、産業における塩素化メタンの生成です。
CH4 + Cl2 → CH3Cl + HCl
ハロゲン付加反応 - 不飽和炭素は、アルケンとアルキンの反応が見られるこの反応の主要部分です。ここで、ハロニウムイオンは、ハロゲンがアルカンと反応する反応における生成物の形成において主要な役割を果たします。ここでは、塩素がエチレンと反応しているのを見ることができます。
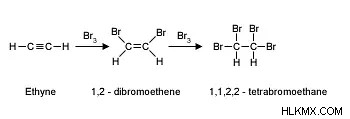
ハロゲン置換 – この反応は主に飽和炭化水素で発生し、反応中にハロゲン原子が水素原子に置き換わります。また、ここに存在するフリーラジカルハロゲンは、一般に炭化水素の処理に使用されます。通常、ハロゲンと飽和炭化水素が見られ、アルカンとハロゲンの反応中に C–H 結合を形成します。
ここに示す例では、1 つのことがわかります。ハロゲンとアルカンを反応させると、ハロゲン化アルキルが生成されますが、この反応では熱の影響が最も顕著です。
CH3CH3 + Cl2 → CH3CH2Cl + HCl
CH4 + Br2 → CH3Br + HBr
ここでは、ルイス酸 (FeCl3 または AlCl3) の存在下でのさまざまな反応を見ることができます。主な例は、置換プロセスまたは求電子ハロゲン化です。
C6H5 – H + Cl2 → C6H5 – Cl + HCl
求電子置換反応 - 主に芳香族ハロゲン化合物を使用し、主な参加者として臭素と塩素が関与する求電子置換プロセス。この反応にはルイス酸が使われます。
2Fe + 3Cl2 → 2FeCl3
2Fe + 3Br2 → 2FeBr3
例
ハロゲンの反応性に応じて、F2> Cl2> Br2> I2 と記述できます。関連する例を次に示します。
塩素との反応 - 塩素とベンゼンの相互作用によりクロロベンゼンが生成されます。これは一般に、塩化鉄または塩化アルミニウムの存在下で行われます。塩素化は、酸素の存在によってかなり遅くなります。
C6H6 + Cl2 → C6H5 – Cl + HCl
フッ素との反応 – フッ素とベンゼンの相互作用により、フルオロベンゼンが生成されます。これは、通常、塩化鉄または塩化アルミニウムの存在下で行われます。
C6H5 -NO2 + F2 → C6H4 – F-NH2
結論
ハロゲン反応は、主に合成化学で非常に重要であり、ポリマーやプラスチック、冷媒、難燃剤、燃料添加物、農産物などの産業で大きなサポートを提供します。さらに、ポリメラーゼ反応の主な要因です。 . PV の製造やジクロロエタンの製造にも必要です。