熱量測定は、内部エネルギーとエンタルピーの変化を測定するために使用されます。この研究分野は、熱化学(サーモは熱を意味します)と呼ばれ、燃料の有効性、さまざまな化学プラントのエネルギーの流れ、化学結合の強さを確認するために使用されます。
熱力学では、化学反応の結果として熱として伝達されるエネルギーの量は、系の内部エネルギーの変化と同一視されることが多く、伝達は系の体積の変化なしに行われていることに注意してください。移動が一定の圧力で発生する場合のシステムのエンタルピー。化学反応によるエネルギーまたはエンタルピーの変化が測定にアクセスできない場合、ヘスの法則によって決定されます。化学反応のエンタルピー変化は、反応全体を分割できる反応の個々のステップのエンタルピー変化の合計。 1822 年、Jean-Baptiste Joseph Fourier は熱伝達に関するフーリエの法則を確立しました。フーリエの熱伝達の法則 は、体を通して伝導される熱の割合は、体内の負の温度勾配に比例すると述べています。
ユニット
カロリーは、1gの水の温度を摂氏1度変えるのに必要な熱量です。キロカロリー(1 kCal =1000 カロリー)は熱の単位です。シリアルの箱の裏に書かれています。カロリーは通常「c」で示され、キロカロリーは「C」で示されます。カロリーは、ジュールであるエネルギーの SI 単位にも関連しています。
1 カロリー =4.184 ジュール。
熱容量は熱量であり、通常ジュールまたはカロリーで表され、システムを摂氏 1 度変化させるのに必要です。物質の比熱容量は、物質 1 グラムを摂氏 1 度上げるのに必要な熱量です。例を考えると、H2O (l) の比熱は 4.18 J/g ° C です。
熱の測定
Cp は一定圧力での比熱容量を表します。
Cv は、一定体積での比熱容量を表します。
特定の温度変化を起こすのに必要な熱量を計算する場合、温度変化、通常物質のグラムまたはモルで与えられる物質の量、熱容量などの特定の情報が必要です。
そして、計算に必要な式は q =mCpΔT ここで、
q =熱量
m =物質の質量
ΔT =温度変化
Cp =比熱/モル熱容量
C =熱容量 (質量に依存しない)
熱量測定の原理
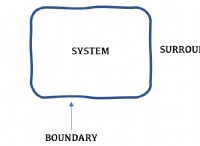
熱量測定の原理は、ある物体から失われる熱と、別の物体から得られる熱に等しいことです。熱量測定に使用される装置は熱量計として知られています。カロリメトリーの主な目的は、化学的または物理的プロセスで伝達される熱エネルギーの量を測定するために使用されますが、システムおよび周囲のプロセス中に発生する温度変化は慎重に測定する必要があります。熱量測定は基本的に、周囲と交換される熱を測定することにより、システムのエネルギーの変化を決定します。
歴史
アントワーヌ・ラヴォアジエは熱量計を、1780 年にモルモットの呼吸からの熱を測定して雪を溶かすために使用した装置であると説明し、1782 年にラヴォアジエとピエール=シモン・ラプラスは、氷を溶かすのに必要な熱を使って氷熱量計を実験しました。化学反応による熱を測定します。
物質の比熱
比熱は、物質 1 グラムの温度を摂氏 1 度上げるのに必要な熱量です。
比熱の式は次のとおりです。
吸収または放出される熱量 =質量 x 比熱 x 温度変化。
物質の比熱容量(Cp)は、物質のサンプルの熱容量をサンプルの質量で割ったものです。比熱は質量熱容量とも呼ばれます。比熱容量の SI 単位は、ジュール/ケルビン/キログラム、J·kg−1·K−1 です。日常生活における比熱の用途のいくつかは、比熱容量の小さい物質であり、フライパン、鍋、やかんなどの調理器具の材料として役立ちます。少量の熱が加えられると、すぐに加熱されます。
結論
熱とは、温度差の結果として、ある高温体から別の低温体に伝達されるエネルギーです。温度の異なる 2 つの物体を一緒にすると、エネルギーが伝達されます。つまり、熱は高温の物体から低温の物体に流れ、一定の安定性が得られます。熱エネルギーは、固体、液体、気体中の原子、分子、またはイオンと呼ばれる小さな粒子の動きの結果です。この 2 つの物体間の移動は熱と呼ばれます。