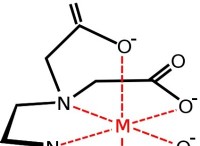
エーテルは、酸素原子が 2 つのアリールまたはアルキル基に結合した有機化学物質であり、同じまたは異なる場合があります。エーテルの標準式は、R-O-R、R-O-Ar、または Ar-O-Ar であり、R はアルキルを表し、Ar はアリール基を表します。
エーテルは一般に、結合した官能基に基づいて 2 つのタイプに分類されます。酸素原子に結合した 2 つの類似した基を持つ対称エーテルと、酸素原子に結合した 2 つの異なる基を持つ非対称エーテルです。エーテルには、さまざまな物理化学的特性があります。エーテル化学反応、化学におけるその意味、およびそれらの分子化合物について説明します。
エーテル
エーテルは、2 つのアリール基またはアルキル基に結合した酸素原子によって定義される有機化合物です。エーテルはアルコールに似た構造を持ち、アルコールもエーテルも水に似た構造を持っています。アルコールでは、アルキル基が水分子の 1 つの水素原子を置換しますが、エーテルの場合、すべての水素イオンがアルキル基またはアリール基で置換されます。
エーテルは、室温で無色の心地よい香りの液体です。エーテルはアルコールよりも密度が低く、水に溶けにくく、融点と沸点が低くなります。それらは主に非反応性であるため、油、脂肪、ガム、ワックス、樹脂、香料、染料、および炭化水素の溶媒として使用できます。特定のエーテル蒸気は、殺ダニ剤、土壌殺虫剤、および燻蒸剤として利用されます。エーテルは、特に麻酔薬として、薬学や医学にも役立ちます. 「エチルエーテル」(CH3CH2OCH2CH3)は、単にエーテルとして知られることもあり、1842 年に外科的麻酔薬として最初に使用されました。「メチルエーテル」またはコデインは、強力な鎮痛剤です。エーテルは非常に可燃性であるため、主に「亜酸化窒素」(N2O) や「ハロタン (CF3CHClBr)」などの可燃性の低い麻酔薬に置き換えられています。
エチルエーテルは、抽出や幅広い化学反応に優れた溶媒です。また、寒冷地でのディーゼルおよびガソリン エンジンの揮発性始動流体としても使用されます。ジメチルエーテルは冷媒であり、スプレー噴射剤です。 「メチル t-ブチル エーテル」は、排気ガス中の窒素酸化物の排出を減らしながらオクタン価を高めるガソリン成分です。エチレングリコール エーテルは、溶媒および可塑剤として利用されます。
エーテルの物理的性質
エーテルには、アルコールに見られるヒドロキシル基がありません。エーテル分子は、鋭く分極した OH 結合を持たない限り、互いに水素結合を形成できません。エーテルには、酸素に 2 つの電子がないなどの障壁があり、NH または OH 結合を持つ他の分子と水素結合を作ることができます。エーテルは、他の分子と一緒に水素原子を生成する傾向があるため、幅広い有機化学物質と驚くほど多くの無機物質の優れた溶媒です。
エーテル分子は互いに水素結合を形成できないため、それらの沸点は同様の分子量のアルコールの沸点よりも大幅に低くなります。たとえば、ジエチル エーテルの沸点は 35 °C / 95 °F ですが、1-ブタノールの沸点は 118 °C /244 °F です。エーテルの沸点は、同様の分子量を持つアルカンにかなり近いです。ペンタンの沸点は 36 °C / 97 °F で、ジエチル エーテルの沸点に近いです。
エーテル化学反応
他のものは主に反応性に対して不活性ですが、幅広い非極性化学分子に対して優れた溶媒特性を持っています。エーテルは溶解力が高く、反応性が低いため、反応を実行するのに適した溶媒です。
エーテルの最も注目すべき反応は、作動酸または HI がそれらと反応するたびに起こる酸触媒による破壊です。この反応は、「求核置換メカニズム」によって行われます。 「一級および二級アルキル エーテル」は SN2 メカニズムを使用して切断しますが、ベンジル、三級、およびアクリル エーテルは SN1 によって分割されます。メチル イソプロピル エーテルと HI の相互作用は、古典的な SN2 反応です。
エーテル酸性切断
SN2 または SN1 メカニズムのいずれかによって、HCl ではなく水素または HI の水性濃度は、エーテルをアルコールとハロゲン化アルキル生成物に分解する傾向があります。エーテルが第一級、第二級、またはメチル アルキル化合物のみに結合している場合、SN2 メカニズムを利用した選択的切断が通常発生します。強酸は最初にエーテル酸素をプロトン化します。得られたハライド共役塩基は、置換基の少ないヒンダード アルキル置換基でプロトン化エーテルに衝突し、ハロゲン生成物が形成されます。より多くの置換基をもつエーテルのアルキル置換基は、脱離基として排出され、アルコール生成物を形成します。
エーテル上のフェニル基は、酸性分解のSN2反応に参加できないことに注意してください。フェニル基が存在する場合、ハライド求核試薬は他のアルキル置換基を優先的に攻撃し、生成物にフェノールが生成されます。
結論
エーテルは反応性が低いため、有用な溶媒です。ほとんどは、臭化水素酸または HBr によって切断されて「臭化アルキル」を生成するか、ヨウ化水素酸によって切断されてヨウ化アルキルを生成します。一方、自動酸化は空気中の化学物質の自然酸化です。エーテルは、酸素の存在下でゆっくりと自動酸化して、ヒドロペルオキシドとジアルキルペルオキシルを生成します。これらの酸化剤は、濃縮または加熱すると爆発する可能性があります。このような爆発を避けるために、エーテルは少量しか調達されず、密閉されたバッグに保管され、できるだけ早く使用されます。