ダルトンの法則のコア コンセプト
1801 年、イギリスの化学者 ジョン ダルトン 蒸気と空気に関する観察を行い、1802 年に出版され、最終的にドルトンの分圧の法則 .このチュートリアルでは、分圧とは何か、ガスの分圧を見つける方法、ダルトンの法則がそれをモル分率に関連付ける方法を学びます。
他の記事で取り上げるトピック
- プレッシャーとは
- シャルルの法則
- アボガドロの法則
- ボイルの法則
- 理想気体の法則
- ファン デル ワールスの状態方程式
- ゲイ・リュサックの法則
- 混合ガス法
複数のガス
1 モルのネオンガスが入ったタンクを考えてみましょう。圧力を 1 気圧とします。ここで、さらにネオン ガスを 1 モル加えたらどうなるか考えてみてください。
プレッシャーに関する記事から、プレッシャーとは 、圧力は容器の壁に衝突するガスの粒子によって引き起こされることがわかっています。ガスのモル数を 2 倍にするとガス粒子の量が 2 倍になるため、この 2 番目のガスのモルを追加すると圧力が 2 倍になることがわかっています。
ここで、別のネオン ガス 1 モルを追加する代わりに、ヘリウム 1 モルを追加するとどうなるかを考えてみましょう。 1 モル中の粒子の量は物質に関係なく同じであるため、追加する粒子の量は以前と同じであることがわかります。
したがって、別のガスを追加すると、タンクの圧力が上昇すると結論付けることができます。
分圧
ネオンとヘリウムを含む前のタンクでは、モルの合計量が 2 モルであり、各モルが 1 気圧を発揮するため、圧力は 2 気圧になります。
この結論から、各種のガスによって加えられる圧力の量は、完全な 2 気圧ではなく、全体の圧力の一部であることがわかります。
ダルトンの分圧の法則
ダルトンの分圧の法則では、これらの部分の合計が容器の全圧力になると述べています。つまり、タンクからのネオンとヘリウムの圧力の合計が、タンクの全圧になります。
これから、方程式が生じることがわかります。 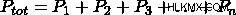 .この方程式はダルトンの法則であり、システムの全圧を決定するために使用できます。
.この方程式はダルトンの法則であり、システムの全圧を決定するために使用できます。
モル分率と分圧
以前は、等量のガスを追加していました。代わりに不均等な部分を追加するとどうなりますか?
前と同じタンクを考えてみましょう。ただし、1 モルのネオンガスの代わりに、元々 3 モルを追加します。アボガドロの法則から、圧力はモル数に比例することがわかっているため、この場合、ネオン ガスの圧力は 3 モルになります。
次に、1モルのヘリウムガスを加えます。現在、ガスの総モル数は 2 倍ではなく、33% 増加しています。このため、コンテナの壁との衝突は 33% しか多くないため、圧力は 1 気圧しか増加しません。
このことから、全体の圧力は 4 atm になり、総モルは 4 mol になることがわかります。ヘリウムガスのモル分率を取ることができます。 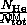 、それが 0.25 に等しいことを確認します。これは、ヘリウムガスによって加えられる圧力の割合でもあります。
、それが 0.25 に等しいことを確認します。これは、ヘリウムガスによって加えられる圧力の割合でもあります。
このため、ガスの分圧は、式によるモル分率によって決定できます。 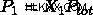 、ここで
、ここで 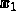 はガス 1 のモル分率です。
はガス 1 のモル分率です。
ダルトンの法則の例の問題
分圧の求め方
ダルトンの分圧の法則に関する問題を解決する方法と、ガスの分圧を見つける方法の例を次に示します。
酸素ガス32gとヘリウムガス12gをタンクに充填する。タンク内の全圧は4気圧です。酸素とヘリウムガスの分圧は?
まず、酸素とヘリウムガスの両方のモル数を決定します。
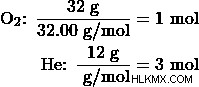
次に、酸素とヘリウム ガスの両方のモル分率を決定します。

最後に、モル分率を使用して分圧を決定します。