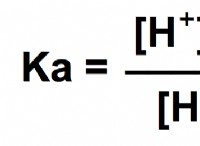溶媒に溶質を加えると、沸点が上がります。不揮発性溶質を含む混合物の沸点は、純粋な溶媒の沸点よりも高くなります。溶質と溶媒の比率は沸点の上昇を決定しますが、溶質の正体は決定しません。したがって、溶液に加えられる溶質の量によって、溶液の沸点がどれだけ高くなるかが決まります。つまり、溶液中の溶質濃度に比例して沸点が上昇します。
集合プロパティのタイプ
- 浸透圧
- 蒸気圧の相対的な低下
- 沸点の上昇
- 氷点下のうつ病
沸点上昇
液体を加熱すると蒸気圧が上がり、大気圧と同じになると液体が沸騰します。
したがって、大気圧が蒸気圧に比例するように、溶液の温度を上げる必要があります。沸点の上昇の意味は、純粋な溶媒の沸点と溶液の沸点との間の不一致として理解されます。
ここで、溶媒の沸点を Tb、溶液の沸点を T とします。したがって、沸点の不一致 (ΔT) は、沸点の上昇として知られています。
沸点上昇の原因は?
- 溶質を溶媒に導入すると、蒸気圧が低下します。この現象は、溶質が溶媒分子を溶解する結果として発生します。
- 溶質が液体の表面で溶媒分子の一部を置き換えるときに、電解液と無電解液の両方で発生します。
- 表面の溶媒分子が少ないため、蒸発が少なくなり、蒸気圧が低下します。
- 蒸気圧を大気圧と等しくするには、より高い温度が必要です。したがって、より高い沸点を考慮することが不可欠です。
沸点上昇の式
溶液の沸点上昇は(ΔTb)で表される。次の式で計算されます:
ΔTb =i*Kb*m
どこで、
- Kb は ebullioscopic 定数です
- m は溶質のモル濃度です
- i は Van’t Hoff 係数です
Kb はしばしば oC/molal または oC.kg.mol-1 で表されます。
この式は揮発性溶媒には適用されず、溶質の濃度が非常に高い場合は精度が低下します。
沸点上昇の式を使用して、溶質の解離度とモル質量を計算できます。
沸点上昇と蒸気圧の関係
沸点の上昇は、蒸気圧で説明できます。
蒸気圧は、溶液分子が気相に入って逃げる傾向の量です。
液体の蒸気圧が気圧と等しくなると、液体は沸騰します。
Kb =RTb2M/ΔHv、
どこで、
- R はガス定数です
- Tb は純粋な溶媒の沸点 [K]
- M は溶媒のモル質量です
- ΔHv は、溶媒 1 モルあたりの蒸発熱です。
結論
特定の溶質が溶媒に導入されると、溶媒の沸点が上昇します。不揮発性溶質でなければなりません。溶液の溶質のモル濃度と沸点の上昇は正比例します。
Tb =Kbm =(1000 w2) (w1 M2)
その結果、沸点の上昇は次のように示されます:
ΔTb =(Kb × 1000 × w2) ÷ (w1 × M2)
その結果、溶質の分子量は次のようになります:
M2 =(Kb × 1000 × w2) ÷ (w1 × △Tb)